发射红或黄色莹光的聚集诱导发射生物探针的制作方法
相关申请
本专利的申请声明于2015年7月16日提交的临时美国专利申请no.62/231,805,于2015年8月27日提交的临时美国专利申请no.62/283,303以及于2015年11月10日申请的临时美国专利申请no.62/285,826,这些申请全部由发明人提交并且通过引用并入本文。
本发明的课题涉及利用红色线粒体靶向聚集诱导发射(aie)探针作膜电位和小鼠精子具活性指标。本发明涉及用于活性氧(ros)检测和相关生物应用(例如炎症成像和葡萄糖测定)的aie-活性荧光探针以及红色荧光aie原的制备和应用。本发明的课题涉及利用红色线粒体靶向聚集诱导发射(aie)探针作膜电位和小鼠精子具活性指标。本发明涉及用于活性氧(ros)检测和相关生物应用(例如炎症成像和葡萄糖测定)的aie-活性荧光探针以及红色荧光aie原的制备和应用。
背景技术:
荧光染料已被广泛应用于现代生物学研究,并促进了荧光显微镜的发展。荧光成像是超强组织观察和观察单个细胞的有力工具,目前为止,在基因表现,蛋白质功能,蛋白质-蛋白质相互作用以及许多其他细胞过程的进展和非侵入性研究中具有重要作用。此外,荧光成像已被证明是研究共混聚合物微观结构的有力工具。远红到近红外(fr/nir)的荧光染料对于体内成像是特别有利的,因为光吸收和自身荧光的效应可以被最小化。由于更长的荧光波长,可以实现更高程度的组织渗透。出于相同的原因,利用fr/nir荧光染料的微观共混聚合物结构的成像不仅可以获得表面图案还有深层的资讯。
关于荧光的分子设计,聚集引导猝灭(acq)效应总是引起光漂白和聚集后荧光强度的衰减,从而限制了长时间监测细胞器和把其性能降低。
2001年发现了显示aie特征的分子。具有aie特性的发光蛋白在分子溶解时几乎不发荧光,但在形成聚集体时变得高度发光。分子内旋转(rir)的限制被认为是aie效应的主要机制。因此,由于限制了分子内运动(rim),aie活性分子在聚集和/或结晶状态下是高度发光的,允许它们在各种领域中应用,例如在oled和生物探针中用于细胞成像和跟踪。aie活性分子已成功应用于生物探针,具有较高的光稳定性和较高的生物相容性。
线粒体是存在于几乎所有真核细胞中的动态细胞器。线粒体形态由一组蛋白质调节。据报导,这些蛋白质的突变与疾病有关,包括神经退行性疾病和心血管疾病。线粒体的主要功能是产生能量,它的95%是真核细胞的主要能量来源,而且atp是由线粒体产生的。
为了合成atp,线粒体不断地氧化底物并在具有大膜电位(δψm)的呼吸电子传递链中的脂质双层上保持质子梯度。δψm是反映线粒体功能状态的重要参数,因此与细胞健康,损伤和功能密切相关。此外,维持线粒体功能至关重要。线粒体δψm是评估精子,男性生殖细胞的生理学,生存力和受精潜力的基本指标。由于线粒体为精子运动提供能量,精子线粒体中的δψm异常可能导致线粒体功能障碍,导致男性不育。因此,开发有效的线粒体形态学检测方法以及δψm对于相关疾病的生物医学研究和早期诊断都具有重要意义。
各种以靶向线粒体阳离子荧光染料已经被开发了,并且可以使用一些染料如罗丹明123(rh123),tmre/tmrm和jc-1来监测线粒体δψm。不过,这些染料的光稳定性由于浓度-猝灭发射效应而变得很不理想。这样的效果只允许于稀释溶液(通常<1-30nm)中使用成像探针,但当激烈的激光束用作激发光源时,也容易导致探针的快速光漂白。
当使用浓度猝灭染料测量δψm时,情况更为复杂。例如,导致线粒体中染料量增加的δψm升高可能导致荧光信号的增强或减弱,这取决于染料浓度是否在非淬灭范围内。jc-1是δψm最广泛使用的荧光指示剂。然而,jc-1对染料负载浓度和时间高度敏感。许多参考文献报导了使用jc-1测量δψm的复杂性和错误结果。因此,开发一种非自淬灭,光稳定的线粒体探针来显示活细胞中的δψm是高度需要的。
通过分子工作,靶向线粒体的aie探针已经成功开发。不过,这些探针中的大多数在短波长区域发射并且对δψm变化没有反应。另一方面,在较长波长区域发射的探针具有各种优点,例如对生物样品的造成最小光损伤,能做到深层组织穿透以及对自发荧光的干扰很小。因此高度希望具有优异的光稳定性和功能的高效红光发射探针。
ros是含有氧的化学反应活性分子。过氧化氢(h2o2)是最著名的ros之一,广泛用于工业和日常生活中的漂洗,漂白和消毒。废水中残留的h2o2水平是国家废物排放标准的重要参数,高浓度的h2o2可能对环境造成氧化损伤。此外,过氧化氢正在成为生物体中常见的分子,因为科学家已经公开了更多的生物过程,其中h2o2参与起着不同的作用。例如,h2o2作为氧化应激的常见指标,在许多组织中诱导抗氧化剂防御,并且是许多酶催化的代谢反应中的生物产物。特别是在葡萄糖氧化酶(gox)的催化作用下,葡萄糖可以转化为葡萄糖酸内酯,同时伴随着h2o2的生成。通过分析酶促产生的h2o2的量,可以间接定量关注的生物分子,例如特定的酶和重要底物(例如葡萄糖)。
另一个重要的ros是过氧亚硝酸盐(onoo-),由于其在生物系统中的多重影响,已经引起越来越多的研究人员的关注。具体而言,当onoo-的生成升高是体内炎症的关键事实。作为一种生物体对病原体或有害刺激物产生的保护性免疫回馈,炎症正成为越来越受欢迎的话题,因为它对癌症,心脏病,糖尿病和阿尔茨海默病等各种主要疾病具有潜在的研究价值。炎症是缺血性心脏病的主要特征,并且是冠状动脉疾病进展的关键机制,其发生在阿尔茨海默病患者脑部的病理脆弱区域。更重要的是,已经确定15-20%的癌症是由慢性炎症引起和诱导的。因此,体内炎症的检测和成像无疑有利于肿瘤转移和扩散前的早期诊断和预防。
现有技术已经报导了许多用于ros检测的荧光探针,例如heecholkang(us20130287689a1),jianghongrao(us20140004049a1)和allankorsgaardpoulsen(wo2008044138a1)已经报导了其实例。一般来说,大多数现有技术参考文献都面临一些问题,如灵敏度低,合成方法复杂,易受环境影响,在溶液中的运作条件有限。
技术实现要素:
在一个实施方案中,本主题涉及具有聚集诱导发射特征的长波长探针,其包含至少一个荧光团,所述荧光团包含以下的骨架结构:
其中,
每个r独立地选自氢,烷基,不饱和烷基,杂烷基,环烷基,杂环烷基,芳基和杂芳基;x是至少一个可与至少一个荧光团共轭的发光体
在一个实施方案中,本主题涉及用于h2o2和onoo-检测的高灵敏度和选择性探针,其包含含有选自以下的主链结构的aie发光蛋白:
其中每个r,r,r“和r'独立地选自由以下组成的组:
,,,,
其中r,r',r“和r”'中的至少一个是。
在一个实施方案中,本主题涉及用于包含aie发光体的h2o2和onoo-检测的高灵敏度和选择性探针,其包含作为主链结构的:
在一个实施方案中,本主题涉及制备本主题的探针的方法,其包括在peg基质中制造aie发光体的纳米颗粒。
在一个实施方案中,本主题涉及用于在uv照射下产生和/或跟踪活性氧物种(ros)的探针,其包含具有以下结构的红色荧光活性氧原子:
在一个实施方案中,本主题涉及用于监测质膜的长期形态变化的探针,所述质膜包含具有以下结构的红色荧光aiegens:
在一个实施方案中,本主题涉及包含近红外aie发光体的探针,其包含以下结构:
在一个实施方案中,本主题涉及用于细胞器靶向的探针,其包含选自以下的红色荧光染料aiegens:
附图说明
图.1a-b显示(a)tpe-in和(b)tpe-ph-in在dmso和dmso/水混合物中具有99%水分数(fw)的发射光谱。染料浓度:10μm;激发波长:450nm。插图:(a)tpe-in和(b)tpe-ph-in在dmso/水混合物中的照片,在365nmuv照射下具有0和99vol%的fw值。
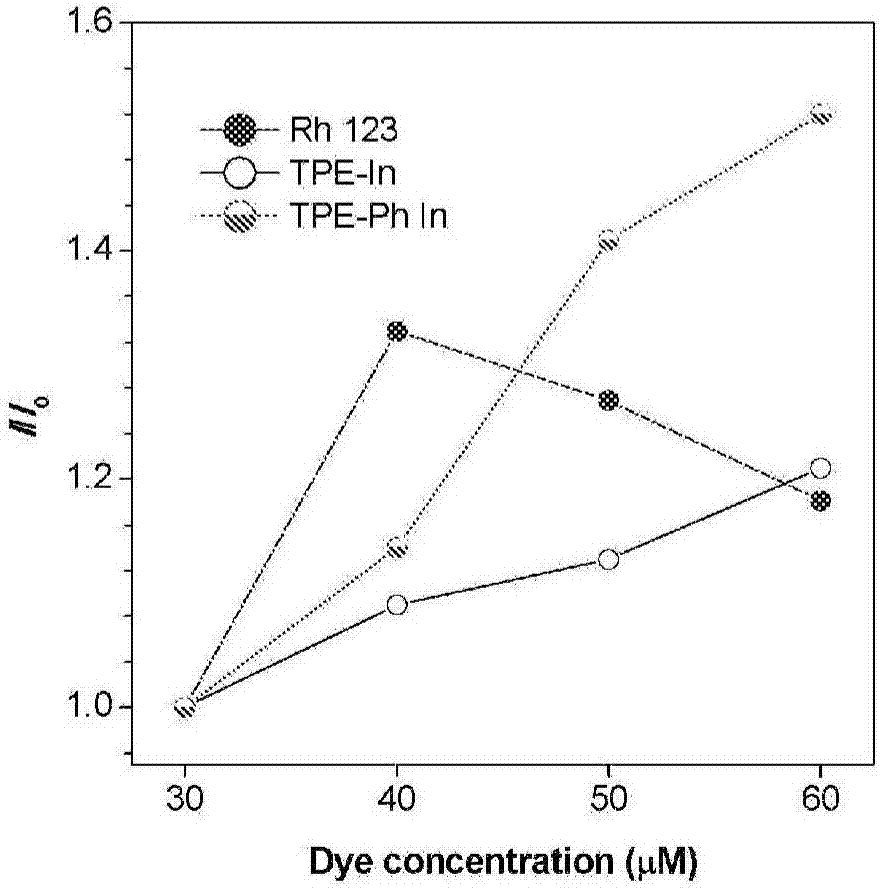
图.2显示rh123,tpe-in和tpe-ph-in在水溶液(1%dmso)中的荧光强度和荧光团浓度之间的关系图。
图.3a-b显示通过mtt测定对hela细胞评价的发光体tpe-in和tpe-ph-in的细胞毒性图。
图.4显示随着扫描次数的增加,tpe-ph-in和mt的荧光强度的信号损失(%)。
图.5a-b显示(a)用10μg/ml寡霉素,然后用20μmcccp处理后用tpe-ph-in(5μm)染色的hela细胞的发射强度的变化。激发波长:488nm。插图:处理兴奋剂期间不同时间段细胞的快照。比例尺:20μm。(b)通过流式细胞术分析未染色的空白hela细胞,未处理的tpe-ph-in染色的hela细胞,寡霉素处理的tpe-ph-in染色的hela细胞和cccp处理的tpe-ph-in染色的hela细胞的荧光强度。
图.6a-d显示了hela细胞的流式细胞术分析(a),用4μmtpe-ph-in染色30分钟(b),用10μg/ml寡霉素处理染色的细胞25分钟(c)或20μmcccp处理25分钟(d)。激发波长:488nm;发射波长:585±11.5nm。
图.7a-b显示tpe-ipb在氘代二氯甲烷中的(a)1hnmrand(b)13cnmr谱。
图.8a-b显示tpe-iph在氘代三氯甲烷中的(a)1hnmrand(b)13cnmr谱。
图.9a-d显示(a)tpe-iph和tpe-ipb在乙腈中的uv光谱。(b)不同分数(fw)的乙腈/水混合物中tpe-ipb的pl光谱。浓度:20μm。(c)tpe-iph在不同分数(fw)的乙腈/水混合物中的pl光谱。浓度:20μm。(d)在549nm处的相对pl强度(i/i0)相对于tpe-ipb的乙腈/水混合物的组成的曲线。
图.10a-e显示了(a)tpe-ipb在乙腈/缓冲液混合物(1:9,v/v;ph10.0)中在37℃下在h2o2(150μm)存在下的时间依赖性pl光谱。(b)在存在和不存在h2o2的情况下tpe-ipb的pl强度对孵育时间的图。插图:照片的解决方案(一)之前和(二)孵化后与过氧化氢在365纳米紫外线照射。(c)tpe-ipb在乙腈/缓冲液混合物(1:9,v/v;ph10.0)中的pl光谱与不同浓度的h2o2在37℃下孵育40分钟。(d)540nm处的pl强度对h2o2浓度的图。溶液浓度:40μm;激发波长:373nm。(e)浸渍在具有不同浓度h2o2的缓冲溶液(10mm,ph=10)中后沉积在滤纸上的tpe-ipb的荧光照片。
图.11显示tpe-ipb在缓冲溶液(10mm,ph=10.0)缓冲液中对不同活性氧的pl响应。[clo-]=100μm,[tbhp]=100μm,[o2·-]=100μm,·oh:在0.1mh2o中20mgfeso4,[100%]=100μm,[1o2]=100μm,[onoo-]=100μm,[h2o2]=100μm)。
图.12a-b显示(a)与gox(2u/ml)和葡萄糖一起温育的乙腈/缓冲液混合物(1:9,v/v;ph10.0)中的tpe-ipb的相对pl强度(i/i0)外加葡萄糖;蓝线:在乙腈/缓冲液混合物(1:9,v/v;ph10.0)中;红线:在含有1%fbs的乙腈/缓冲液混合物中。插图:在相同条件下葡萄糖测定的线性校准曲线。(b)tpe-ipb在乙腈/缓冲液混合物中对不同糖的pl响应。溶液浓度:40μm;孵育时间:1小时;孵育温度:37℃;[gox]:2u/ml;[gal]:1mm;[man]:1mm;[fru]:1mm;[lac]:0.5mm;[suc]:0.5mm;[dex]:0.18mg/ml;[glu]:1mm。插图:与在365nm紫外光照下拍摄的不同糖类孵育的溶液的照片。
图.13显示在与200μm的onoo-(红色条)和h2o2(绿色条)在不同的ph值下温育时,536nm处的tpe-ipb(40μm)的pl强度变化。
图.14a-d示出了(a)tpe-ipb的示意图纳米探针和onoo-他们的“启动”感测。(b)在日光下在pbs缓冲液(ph7.4)中的tpe-ipb聚集体和tpe-ipb纳米探针的照片。(c)通过dls测量的tpe-ipb纳米针和pbs缓冲液中的tpe-ipb聚集体的尺寸分布。(d)tpe-ipb纳米探针的tem图像。
图.15a-d显示(a)i/i0相对于pbs缓冲液(ph7.4)中的各种rons的图。i0和i分别是在0和400μm的rons浓度下tpe-ipb纳米探针溶液的pl强度。(b)用不同浓度的onoo-处理的tpe-ipb纳米探针的pl光谱。(c)分别加入onoo-后tpe-ipb纳米针和tpe-ipb聚集体的时间依赖性pl相对强度(i/i0)。i0和i分别是在用400μmonoo-处理后,在不存在rons的情况下和在不同时间点的纳米探针/聚集体溶液的pl强度。(d)在持续照射10分钟的mcf-7细胞中tpe-iph纳米探针,qd565和fitc之间的光稳定性比较。i0和i分别是不同时间点样品的初始pl强度和pl强度。
图.16a-b显示(a)具有(对角线)和没有(固体)tpe-ipb纳米探针施用的小鼠的血液测试参数(每组n=4)。治疗组和未治疗组之间没有统计学显著性差异。(b)来自tpe-ipb纳米探针注射的健康小鼠的h&e染色的肝脏,脾脏和肾脏切片的典型图像。
图.17a-e示出了(a)申请特定体内炎症成像aie点亮纳米探针的示意图。(b)在指定的时间间隔内静脉内注射tpe-ipb纳米探针之前和之后,mrsa感染诱导的带有炎症的裸鼠的体内非侵入性荧光图像。白色圆圈表示炎症区域。(c)用tpe-ipb纳米探针处理3小时后带有炎症的小鼠的各种组织的离体荧光图像。(d)各种组织中荧光强度的半定量分析。*表示与其他组织相比的统计学显著性(p<0.05)。数据表示为平均值±标准偏差(n=5)。(e)来自tpe-ipb纳米探针处理的小鼠的感染和未感染的皮肤组织切片的代表性clsm图像。血管通过血小板/内皮细胞粘附分子1(pecam-1,红色荧光)进行免疫染色。
图.18a-f显示(a,b)mrsa和大肠杆菌感染的小鼠在(a)万古霉素和(b)青霉素治疗之前和之后的指定时间间隔的体内非侵入性荧光图像。tpe-ipb纳米探针分别在抗生素治疗前和治疗后7天和14天静脉注射到小鼠中。(c,d)用(c)万古霉素和(d)青霉素处理14天的小鼠感染部位的h&e染色切片的典型图像。(e,f)用(e)万古霉素和(f)青霉素处理14天的小鼠的感染部位切片的典型clsm图像。tpe-ipb纳米探针在第14天注射,血管通过pecam-1免疫染色。
图.19显示化合物6a在二甲基亚碸溶液中的吸收光谱。
图.20显示化合物6b在二甲基亚碸溶液中的吸收光谱。
图.21显示化合物6c在二甲基亚碸溶液中的吸收光谱。
图.22显示化合物12在二甲基亚碸溶液中的吸收光谱。
图.23a-b显示了(a)化合物6a在甲苯/二甲基亚碸混合物中不同甲苯分数(ft)下的pl光谱。(b)i/i0与ft的关系图i=在650nm处的纯二甲基亚碸溶液中6a的pl强度;浓度:10μm;激发光:460nm。
图.24a-bs显示了(a)化合物6b在甲苯/二甲基亚碸混合物中不同甲苯分数(ft)下的pl光谱。(b)i/i0与ft的关系图i=在650nm处的纯二甲基亚碸溶液中6b的pl强度;浓度:10μm;激发光:460nm。
图.25a-b显示了(a)化合物6c在甲苯/二甲基亚碸混合物中不同甲苯分数(ft)下的pl光谱。(b)i/i0与ft的关系图i=在650nm处的纯二甲基亚碸溶液中6c的pl强度;浓度:10μm;激发光:460nm。
图.26a-b显示了(a)化合物12在甲苯/二甲基亚碸混合物中不同甲苯分数(ft)下的pl光谱。(b)i/i0与ft的关系图i=在650nm处的纯二甲基亚碸溶液中12的pl强度;浓度:10μm;激发光:460nm。
图.27显示化合物16在四氢呋喃中的吸收光谱。
图.28显示化合物17在四氢呋喃中的吸收光谱。
图.29a-b显示了(a)具有不同水分(fw)的四氢呋喃/水混合物中的化合物16的pl光谱。(b)相对pl强度对fw的图。i0是四氢呋喃中染料在580nm处的pl强度;染料浓度:10μm;激发波长:410nm。
图.30a-b显示了(a)具有不同水分(fw)的四氢呋喃/水混合物中的化合物17的pl光谱。(b)相对pl强度对fw的图。i0是在四氢呋喃中染料在680nm处的pl强度;染料浓度:10μm;激发波长:525nm。
图.31a-b显示(a)在hepesph7.4缓冲液中在1%二甲基亚碸中与不同磷脂,dna和rna混合的化合物6a的uv光谱和(b)pl光谱。浓度:10μm;激发波长:460nm。
图.32a-b显示化合物6a与dna的pl光谱,并用(a)dnase和(b)rnase在hepesph7.4缓冲液中处理。浓度:10μm;激发波长:460nm。
图.33a-e显示用(a和c)化合物6a和(b和d)sytornaselect染色的hela细胞在连续激发下获得的共焦图像。(e)用ascp或sytornaselect染色的hela细胞的fl信号损失增加。扫描。6a:激发波长:560nm,发射波长:650-750nm;sytornaselect:激发波长:488,发射波长:500-600nm。
图.34显示用不同浓度的化合物6a染色8小时的hela细胞的mtt测定活力。数据表示为五个独立试验的平均值。
图.35在共焦图像中显示pl光谱,其中○:脂滴中的pl信号;△:脂滴外的pl信号。
图.36显示纳米粒子平台调查和建议的应用。
图.37a-b(a)显示了tpe-tetrad上苯基的分子转动(b)在tetrad含有不同体积分数水的thf/水混合溶液中,紫外灯下的照片。
图.38a-b.(a)tpe-tetrad在不同水分的thf/水混合物中的pl光谱。(b)是相对pl强度(i/i0)曲线。其中,i0是染料在thf溶液中在668nm的光强。染料浓度:10μm;激发波长:488nm;内嵌的图片分别是(a)tpe-tetrad水的含量和(b)薄膜照片。
图.39a-b(a)tpe-tetrad生成ros的能力(b)评估tpe-tetradpeg纳米颗粒在有无白光条件下的ros细胞毒性的mtt测定。
图.40显示msn@aie合成的示意图;插图是tem(透射电子显微镜)下溶液颗粒的荧光和形态。
图.41a-b(a)用动态光散射法测定且比较tpe-tetrad纳米聚集体及其msn封装物的流体动力学直径(b)tpe-tetrad纳米粒子和msn包裹tpe-tetrad的纳米粒子的光致发光谱。
图.42显示了tpe-tetrad/aunppeg纳米颗粒共轭物的示意图。插图在tem下显示aunps形态。
图.43a-g(a-c)与mito-tracker探针的共染色;(d-f)在clsm(共聚焦激光扫描显微镜)下,用dcfh(二氯荧光素)为ros指示剂展示不同处理的a549癌细胞,细胞内ros水平;(d)探针+,光照-;(e)探针+,光照+;(f)探针+,光照+,乙酰半胱氨酸+;(g)各种不同处理后a549细胞的细胞活性。
图.44a-d(a)不同处理时菌落的形成;(b)(a)的菌落分析的定量数据。(p<0.01);(c)用不同的常用的放射增敏剂治疗后的菌落形成;(d)c的菌落分析的定量数据。(p<0.01)
图.45a-c展示蛋白质印迹法分析(a)p-erk,erkp-aktandakt;(b)不同处理的a549细胞的bcl-xl,bcl-2,bad和caspase-3;(c)表明化合物6b如何作为一种有效的放疗增敏剂的一个示意图。
图.46a-b显示hela细胞的共聚焦图像在化合物12(3.5μm)染色5分钟之前(伪红色),加入(a)hg2+(100μm)之后(伪绿色)和(b)对照组染色40分钟,条件控制:λ激发=488nm和λ发射=600-750nm。
图.47显示了胰蛋白酶处理后hela细胞的形态变化。
图.48a-h显示用化合物12(3.5μm)染色5分钟hela细胞的明场合并的共聚焦图像,(a)没有胰蛋白酶处理而(b-h)胰蛋白酶处理不同时间。插图:没有明亮的放大图像。条件:λ激发:488nm,λ发射:600-750nm。
图.49显示用化合物6c(4μm)和h2dcfda(10μm)共染色的hela细胞,用405nm光的照射不同时间下的共聚焦图像。条件:aie-mem-ros:λ激发:405nm,λ发射:500-600nm;pi:λ激发:488nm,λ发射:490-650nm。
图.50显示用合物6c(4μm)和pi(3μm)共染色的hela细胞,用405nm光的照射不同时间下的共聚焦图像。条件:6c:λ激发:405nm,λ发射:500-600nm;pi:λ激发:560nm,λ发射:580-740nm。
图.51展示在650nm激发的荧光强度的变化的共聚焦图像。
图.52化合物6c在黑暗中培养hela细胞(黑色)和用白光照射预处理2分钟并随后ascp-tpa在黑暗中培养的hela细胞(灰色)的细胞活性。
图.53a-c(a)显示了tpe-py-ncs(10μm)在不同己烷含量的thf/己烷混合液(fh)中的pl光谱。(b)光谱峰强与fh值的关系曲线。插图:用365nm的手持紫外灯照射下的,tpe-py-ncs在不同fh值的thf/己烷混合物中的照片(c)tpe-py-ffgysa(1μm)和tpe-py-ysa(1μm)在加和不加入pc-3细胞裂解物的pbs缓冲液中的pl光谱。对于(a-c)激发波长在405nm。
图.54a-d显示激光共聚焦扫描显微镜图像:(a)pc-3癌细胞(b)用单克隆抗epha2蛋白的抗体/alexafluor633共轭次级抗体染色后平滑肌细胞。(c)和(d)分别是(a)和(b)的相应的荧光/透射的叠加图像。
图.55a-i显示激光共聚焦扫描显微镜图像:(a)tpe-py-ffgysa和(b)抗epha2蛋白的抗体/alexafluor633标记的二抗co染色pc-3肿瘤细胞。这些细胞用tpe-py-ffgysa在37℃下90分钟。(c)是(a)和(b)的重叠图像。在0℃下用tpe-py-ffgysa(d)培养1小时后pc-3癌细胞的clsm图像,随后在37℃下进一步温育细胞(e)10分钟和(f)60分钟。(g-i)分别是(d-f)的相应的荧光/透射的叠加图像。(a-i)的[tpe-py-ffgysa]=1μm。
图.56a-ba.在37℃下的游离态ysa肽(500μm)预处理的pc-3癌细胞在tpe-py-ffgysa(1μm)培养90分钟后的clsm图像。(b)是(a)的相应的荧光/透射对的叠加图像。
图.57a-h显示在37℃下,tpe-py-ffgysa培养90分钟后,(a)平滑肌细胞,(b)pc-3癌细胞的clsm图像。(c)pc-3癌细胞和(d)平滑肌细胞在tpe-py-ysa在37℃下培养90分钟后的clsm图像。(e-h)分别是(a-d)的相应的荧光/透射的叠加图像。[tpe-py-ffgysa]=[tpe-py-ysa]=1μm。
图.58a-c显示(a)dcf在530nm处的荧光强度(fi)(b)在添加和不添加维生素c(vc)的水溶液中,dpbf在418nm处的相对吸光度对于tpe-py-ffgysa(1μm)的光照射时间的函数。(c)clsm图像显示用dcf-da作为ros指示剂指示经过不同处理的pc-3细胞的细胞内ros水平。将细胞在37℃用tpe-py-ffgysa(1μm)培养90分钟。光照射(0.1wcm-2)进行2分钟。[nac]=1mm。
图.59a-c(a)分别用tpe-py-ffgysa(1μm)和光照射处理48小时后的pc-3癌细胞和平滑肌细胞的细胞活性。(b)在加入32nmptx24小时后,用tpe-py-ffgysa(1μm)培养的pc-3癌细胞的细胞活性。分别在ptx添加后的第0,3,6,9,12小时进行单光照射(0.1wcm-2,2min)。(c)在加入不同浓度的ptx48小时后,pc-3细胞接分别用tpe-py-ffgysa(1μm)和光照处理后,pc-3癌细胞的细胞活性。对于(a)和(c),分别在ptx添加后12,24和36小时(对于a来说ptx=0nm)进行三次光照射(0.1wcm-2,2min),数据表示为平均值±s.d。(b)-(c)中的**分别相对于单独的ptx组(探针-;光-),p<0.01。
图.60a-c显示(a)不同方法处理后的pc-3癌细胞中各种蛋白质表达的蛋白质印迹分析。(b)在存在和不存在nac的情况下进行蛋白质印迹分析。(c)基于蛋白印迹数据提出的协同机制的示意图。
具体实施方式
定义:
提供以下定义是为了理解本主题和构建所附专利权利要求。
注意,除非上下文另有明确说明,否则在本说明书和所附权利要求书中所使用的单数形式“a”,“an”和“the”也同样包括复数形式,除非上下文另有明确说明。
“聚集诱导发光”是指聚集形成或固态时荧光/磷光开启。当分子溶解,材料是不发射。但是,当分子内旋转受到限制时,发射开启。
“发射强度”是指通常从荧光光谱仪或荧光显微镜测量获得的荧光/磷光的量值。
“荧光团”是指显示荧光的分子。
“激活法光”是指显示发冷光的分子。
“aiegen”是指表现出aie特征的分子。
除非另外定义,否则本文使用的所有技术和科学术语具有与目前描述的主题所属领域的普通技术人员通常理解的相同的含义。
如果提供一系列值(例如浓度范围,百分比范围或比率范围)应该理解为除非上下文另外清楚地指出,在该范围的上限和下限之间以及在该陈述范围内的任何其它陈述的值或中间值,每个中间值至下限单位的十分之一都包含在所描述的主题内。
这些较小范围的上限和下限可以独立地包括在较小的范围内,并且这样的实施例也包含在所描述的主题内,受限于所述范围内的任何特别排除的限制。在所述范围包括一个或两个限制的情况下,所述主题中也包括排除那些所包括的限制中的任一个或两个的范围。
在整个申请中,各种实施例的描述使用“包含”语言;然而,本领域技术人员将理解的是,在一些特定情况下,可以替代地使用语言“基本上由......组成”或“由......组成”来描述实施例。
为了更好的理解本教程并且绝不限制该教程的使用范围,除非另有说明,否则表述数量,百分比或比例的所有数字以及说明书和权利要求书中使用的其它数值都是大约的,需要修正一下。因此,除非有相反的指示,否则在以下说明书和所附权利要求中阐述的数值参数,都是不是准确值,需要根据所期待的性质而变化。至少,每个数值参数应至少根据报告的有效数字的位数和四舍五入法来解释。
缩略词
aee聚集增强发光
aie聚集诱导发光
acq聚集引起淬灭
ascp(z)-4-(4-(1-氰基-2-(4-(二甲基氨基)苯基)乙烯基)苯基)-1-甲基吡啶-1-六氟磷酸盐(v)
aunp金纳米粒子
cams细胞粘附分子
cccp羰基氰化3-氯苯腙
clsm激光共聚焦扫描显微镜
dcf二氯荧光素
dcf-da2’,7’-二氯荧光素二乙酸酯
dmem达尔伯克改良伊格尔培养基
dmso二甲基亚砜
dna脱氧核糖核酸
dnase脱氧核糖核酸酶
dpbf1,3-二苯基异苯并呋喃
dppe二棕榈酰磷脂酰乙醇胺
e.coli大肠杆菌
epr提高透气性和滞留性
fbs胎牛血清
fitc异硫氰酸荧光素
fr/nir远红外到近红外
gnp金纳米粒子
gox葡萄糖氧化酶
h&e苏木精-伊红
h2o2过氧化氢
hrms高分辨质谱
i/i0相对峰强度
lc液相色谱
lod检测限
lps脂多糖
madli-tof基质辅助激光解吸电离源-飞行时间
mito-gfp
mrsa耐甲氧西林金黄色葡萄球菌
mt红色线粒体探针fm
mtr红色线粒体探针cmxros
mtt3-(4,5-二甲基-2-噻唑基)-2,5-二苯基溴化四唑
nacn-乙酰半胱氨酸
nir近红外
nmr核磁共振
oled有机发光二极管
onoo-过氧亚硝基阴离子
pbs磷酸盐缓冲液
peg聚乙二醇
pet光致电子转移
pl光致发光
pma12-豆蔻13乙酸佛波醇
ptx紫杉醇
raw264.7巨噬细胞
rim分子内运动受限
rir分子内转动受限
rna核糖核酸
rnase核糖核酸酶
rons活性氧氮物种
ros活性氧
tbhp叔丁基过氧化氢
tem透射电子显微镜
tict扭曲内部的电荷转移
tocl四油酸心磷脂
tpe四苯乙烯
tpe-iph2-(((4-(1,2,2-三苯乙烯基)苯基)氨基)甲基)苯酚
tpe-tpp四苯乙烯-三苯基磷
uv紫外
δψm膜电位
aie红光靶向线粒体分子探针作为指示剂研究细胞膜电位与小鼠精子活性。
在实例中,本发明涉及一种发红光的长波分子并用它染色线粒体,监测线粒体膜电位和小鼠精子活性。特别是,本发明涉及具有aie和aee特性的tpe衍生物的发光分子并且使用它们追踪细胞内线粒体膜电位变化和评估精子活力。本发明涉及将杂环分子和aie分子通过乙烯基功能化连接制备阳离子发光材料。这些阳离子发光材料展现出长的波长发射和聚集诱导发光的性质。
在实例中,本发明主要针对具有诱导发光特性至少包括一个荧光基团的长波长探针分子,包括有以下骨架结构的分子:
在这
每个r基团可以单独的被选从氢,烷基,不饱和烷基,环烷基,杂烷基,杂环烷基,芳基,芳基杂环和x是含有至少一个带有共轭体系的荧光基团的发光基团。
在实例中,该发明涉及的荧光团具有如下骨架结构:
在这
r1,r2,r3,r4,和r5可以单独选择从以下的基团中:cnh2n+1,c10h7,c12h9,oc6h5,oc10h7,oc12h9,cnh2ncooh,cnh2nncs,cnh2nn3,cnh2nnh2,cnh2ncl,cnh2nbr,cnh2ni,和;
r’可以单独选择从以下的基团中:cnh2nncs,cnh2nn3,cnh2nnh2,cnh2ncl,cnh2nbr,cnh2ni和;
x1可以单独选择从以下的基团中:i,cl,br,pf6,clo4,bf4,bph4,和ch3phso3;且
n=0to20.
在实例中,目前主题的探针用于标记活细胞中的线粒体。在一个实施例中,本主题的探针来指示线粒体膜电位的变化。在一个实施例中,本主题的探针用于原位监测活细胞中的一个δψm的变化。在一个实施例中,本主题的探针通过监测小鼠精子细胞和精子活力的细胞膜电位的不同,来评估精子活力。
在一个实施例中,特定光激发的tpe-in在dmso溶液中694nm处发较弱的光。当溶剂中的水含量达到99%时,观察到较强的红色荧光。对于tpe-ph-in(图.1).aie效应更加明显。由于聚集体形成tpe-ph-in的发光提高约70倍。tpe-in和tpe-ph-in都是aie分子,因此是没有遇到最常规的线粒体探针(如rh123)的自猝灭问题。(图.2)
在一个实施例中,这两种发光分子对hela细胞的细胞毒性评估使用四甲基偶氮唑盐(mtt)法。如图3所示,当将5μmtpe加入到hela细胞中时,细胞存活率显著降低。相比之下,tpe-ph-in几乎没有细胞毒性。即使在培养基中tpe-ph-in浓度在8μm时,细胞生长也没有明显影响。tpe-in的平面化可以促进分子与dna相互作用,从而导致更高的细胞毒性。
tpe-in具有更好的平面;tpe单元的一个苯环与吲哚单元共面,而tpe-ph-in更多采用一种的扭曲的构像。tpe-in和tpe-ph-in的化学结构如下:
由于它的构象,tpe-ph-in被选定做细胞染色试验。预实验表明该染料具有细胞渗透性,能够特异性地染色线粒体。与紫外下发蓝光aie线粒体探针tpe-tpp(四苯基乙烯三苯基膦),tpe-ph-in可以用488nm激光激发,因此与激光共聚焦显微镜更兼容,体现更高的信噪比。为了测试tpe-ph-in线粒体选择性,与商业
此外,揭示了利用小的有机染料在荧光蛋白上进行细胞染色的优点。在共染实验中,观察到的细胞都均匀沾上红色发光的tpe-ph-in,而mito-gfp的绿色通道成像中,几个细胞发出的光明显弱于其他的一些。这是由于不均匀的转染率和线粒体细胞mito-gfp表达水平的不同,这些也被提到在mito-gfp的用户手册中。探讨tpe-ph-in稳定性,被tpe-ph-in染色的细胞由共聚焦显微镜连续扫描。40次扫描后,tpe-ph-in的信号损失小于原始光强的10%,第一次和第四十次荧光图像之间没有显著性差异。然而,当mitotrackerredfm(mt),商业上的红色发射线粒体探针,是相同的激发功率下进行测试(图4),mt的荧光信号的损失高达初始值的90%并且几乎没有荧光在扫描8次后。毫无疑问,tpe-ph-in具有比商业mt更高的光稳定性,这意味着它有长期的线粒体成像与形态分析的能力。
δψm是阳离子的亲脂性染料进入并染色线粒体的主要驱动力,所以线粒体的功能可以通过用对δψm敏感的探针被检测。对测试tpe-ph-in对δψm的变化的响应,膜电位的兴奋剂,寡霉素和羰基氰-3-氯苯腙(cccp)在染色过程之前分别用来增加或减少δψm,当细胞经寡霉素处理,观察红色荧光信号显著增强。一旦细胞经cccp,tpe-ph-in不再能有效地在线粒体中积累,导致荧光信号的降低。结果表明,tpe-ph-in在线粒体中积累取决于δψm,更重要的是,荧光信号值可以直接表示基于荧光强度和线粒体中的染料浓度呈正相关关系的δψm,这个对传统染料的浓度猝灭效应来说是难以实现。
进一步检验tpe-ph-in在跟随活细胞中δψm原位实时改变的可行性,依次加入不同的兴奋剂,然后通过激光共聚焦显微镜观察荧光强度和荧光成像。首先用5μm的tpe-ph-in对hela细胞进行30分钟染色(图5a)。观察到线粒体发红光。比细胞中加入10μg/ml的寡霉素时的荧光信号增加了1.5倍。线粒体的增强发射信号可以保留一段时间。再添加20μmcccp进入培养基,立即导致发光强度急剧降低。如上所述,寡霉素和cccp处理可分别增加和减少δψm,这反映在tpe-ph-in荧光信号的变化。由于高信噪比和低背景,在整个过程中不需要清洗步骤,从而为活体细胞微环境变化的跟踪提供了一种方便的方法。
为了探索tpe-ph-in在高通量分析中的应用,流式细胞仪被添加到研究中。hela细胞染色4μmtpe-ph-in在30分钟(图6b)表现出的平均荧光强度的2866左右这可以很容易区分的未染色细胞(图6a)。根据共聚焦图像的结果,当细胞被加入寡霉素25min,在平均荧光强度略有增加(图6c)。形成鲜明对比,cccp和tpe-ph-in染色细胞25min,平均荧光强度下降5.4倍(图6d),这也与激光共聚焦显微镜采集的结果一致。平均强度绘制在图5b。流式细胞仪的使用提供了一个可以探讨tpe-ph-in在不同环境下细胞的高通量定量分析方式。
利用tpe-ph-in良好生物相容性和膜电位依赖性,探索了评价精子活力的可行性。小鼠精子细胞在5μmtpe-ph-in中1h,荧光显微镜下,精子中段可以见到不同程度的荧光强度的。为了进一步了解这种现象,跟踪和记录tpe-ph-in染色精子的动态运动。结果表明,明亮的红色荧光来自高能精子,而非活精子只发出微弱的红色荧光,甚至不发光。染色线粒体内tpe-ph-in的荧光强度反映了线粒体的流动性,展示出tpe-ph-in是一种很有前途的荧光探针,用于监测精子的功能。
aie活性荧光探针检测活性氧及相关生物应用
在另一个实施例中,本发明涉及一种对h2o2和onoo-高灵敏度、高选择性的检测探针,具有aie特性的骨架结构包括以下几种:
其中每个r,r′,r”,和r”’是独立地选自从以下基团中:
,,,,
在这r,r’,r”和r”’中至少一个是。
在一个实施例中,本发明涉及一种对h2o2和onoo-高灵敏度、高选择性的检测探针,具有aie特性分子作为骨干结构:
在一个方案中,本主题结构做为一个针对h2o2和onoo-基团的高灵敏性及选择性aie发光体的骨干结构:
在一个方案中,本主题探针可用于检测缓冲溶液及血清样品中的葡萄糖。在某方案中,本主题涉及的探针可能处于聚集状态或固体状态。在某方案中,aie发光体被用作体内炎症的显像剂。
在一个方案中,本主题结构可用于在peg基质中制备基于本结构的aie发光体的纳米颗粒。
同时,本主题结构证实可作为有效及优越的检测ros的aie探针的模板化合物,特别是tpe-ipb和tpe-iph探针。tpe-iph由三部分组成:tpe作为荧光基团,亚胺作为发射介质,以及作为ros识别位点的苯基硼酸酯。探针在溶液状态和聚集状态下都不发光,但在h2o2或onoo-存在时可发出强烈的黄色荧光。由于gox可催化d-葡萄糖发生氧化反应产生h2o2,所以该探针可以通过定量酶促反应产生的h2o2,间接地检测葡萄糖浓度。tpe-ipb纳米探针可以作为具有高选择性及对比度的体内炎症成像探针,同时具有能将抗炎剂在体内的治疗功效可视化的特点。
tpe-ipb和tpe-iph的合成路线如下:
在温和条件下,通过tpe-nh2(1)和苯基硼酸酯改性的苯甲醛(2)之间的缩合反应合成tpe-ipb。tpe-ipb的化学结构通过标准光谱技术nmr和hrms(图7a-b)确认,其质量为667.3258。
虽然tpe是一种众所周知的易合成分子,其量子效率高,在聚合状态或固体状态下具有良好的光稳定性,但是如何调节tpe的发射,特别是在分子水平上,仍然是一个挑战。如本文所示,亚胺基团(c=n)能够猝灭tpe的发射。有两种理论可以解释其淬灭机制。一个理论涉及光致电子转移(pet)的过程,既通过电子从供体轨道转移到受体轨道来阻止辐射衰变。另一个理论是c=n的顺反异构化过程,它作为从激发态到基态的非辐射衰变的通道。因此,由于亚胺的存在,tpe-ipb在聚合状态下被淬灭。此外,还将含有ros响应性可裂解基团的苯基硼酸频那醇酯部分引入到tpe-ipb中。当存在ros时,特别是h2o2和onoo-,苯基硼酸频那醇酯发生氧化反应被切割,然后释放出小分子。在中性条件下,tpe-ipb与h2o2或onoo-反应后的残留结构将被质子化并转化成2-(((4-(1,2,2-三苯基乙烯基)苯基)亚氨基)甲基)苯酚(tpe-iph)。用于h2o2和onoo-检测的tpe-ipb的结构设计如下:
对于tpe-iph,假设其在羟基的质子和亚胺上的孤电子对之间可形成分子内氢键。基于上述两种理论基础,分子内氢键的形成将使氮原子孤对电子被同时定位和锚定,并固定亚胺构象,导致的亚胺淬灭效应的显著抑制。此外,tpe-iph同时具有aie特征:即,尽管形成了分子内氢键,由于苯环的动态旋转tpe-iph在稀溶液中保持无荧光状态,但通过rim机制在聚集状态下发出强烈荧光。
为了验证该假设,根据上述合成路线合成tpe-iph分子。通过nmr和hrms(图8)确定合成得到的tpe-iph的纯度和特性,其精确质量为451.1936。tpe-iph是tpe-ipb与h2o2反应后的预期产物,首先研究了tpe-iph和tpe-ipb的光学性能。
如图9a所示,tpe-iph和tpe-ipb在乙腈中的吸收光谱分别显示在373nm和347nm处出现最大吸收值。tpe-ipb的吸收峰红移是由分子内氢键结合引起的,它造成c=n结构的构型固定,使得两个苯环与亚胺相连接更加平坦,导致整个分子有更好的结合。由于tpe-iph和tpe-ipb都含有tpe结构,因此在乙腈/水混合物中进一步验证它们的aie特征。对于tpe-ipb分子,当向其乙腈溶液中加入水时,其光致发光(pl)强度保持在一个较低水平,并且在光谱上没有明显的峰出现(图9b)。这归因于未锚定的亚胺基团存在的pet效应或顺式/反式异构化过程,导致即使在聚集状态下它也可以淬灭tpe的发射。将乙腈/水混合物中的含水量从0增加到60%时,tpe-iph的pl强度仍然很弱。然而,此时进一步向混合物中加入水会导致pl强度的急剧且显着的增强。当含水量达到90%,此时溶液的黄色荧光比纯乙腈溶液中强30倍以上(图9c和9d),这清楚地表明tpe-iph具有aie特性。
和葡萄糖的荧光检测
首先优化了从tpe-ipb得到tpe-iph的裂解反应过程的温育时间条件。加入150μm的h2o2后,每2分钟记录一次tpe-ipb的pl光谱。如图10a和10b所示,tpe-ipb在540nm处的荧光强度随温育时间延长而逐渐增加,而不加h2o2的对照组几乎不发光。当与h2o2孵育达40分钟时,pl强度达到平台期,表明此时裂解反应接近饱和状态。
由于tpe-ipb通过h2o2转化为tpe-iph是一个可化学计量的过程,这为建立定量检测h2o2工作曲线的创造了可能性。因此,利用不同浓度的h2o2进行实验。如图10c所示,随着h2o2浓度从0增加到200μm,540nm处的pl强度逐渐增加。与h2o2的浓度相应的pl峰强度绘制在图10d中,其在0~100μm范围内呈线性关系,相关系数0.999。h2o2的检测限(lod)约为100nm(s/n=3,n=11)。由于选择性是传感技术的一个重要参数,进一步研究了tpe-ipb对其他类型ros的pl响应。图11说明h2o2可诱导pl强度的显著增强,但onoo-对检测系统存在一定的干扰,因为苯基硼酸频那醇酯结构也响应于onoo-。相同条件下,包括次氯酸根,叔丁基氢过氧化物(tbhp),单线态氧和羟基等在内的其它ros则几乎不会影响tpe-ipb的pl强度。
由于tpe-ipb在悬浮聚集状态下检测h2o2时表现出的良好性能,进一步考虑了其在固态下检测h2o2的可能性。将tpe-ipb沉积滤纸浸入含有不同h2o2浓度的缓冲溶液(ph10.0)中,温育40分钟后取出。可以明显观察到浸入了较高h2o2浓度溶液中的滤纸发光更强(图10e),结果表明tpe-ipb沉积试纸可作为h2o2指示剂。该现象说明,由于tpe-iph的aie特性,tpe-ipb在不同反应条件下具有广泛的适应性。
由于成功实现了对h2o2的定量检测,所以基于tpe-ipb探针的后续系列应用是可实现的。例如,众所周知,当存在gox时,d-葡萄糖将被氧化为葡糖酸内酯,同时伴随着h2o2的生成。而且,该过程中产生的h2o2的量与葡萄糖的量成比例。因此,当探针溶液中共同存在gox时,tpx-ipb可以通过量化h2o2的浓度来间接检测d-葡萄糖。如预期的那样,当葡萄糖浓度逐渐增加并且其饱和强度比初始水平高10倍时,tpe-ipb的pl强度增强。相对峰值强度(i/i0)如图12a(白色点)所示,结果表明tpe-ipb与葡萄糖浓度在0-200μm范围内呈现良好的线性关系。
另一个可能的应用是针对糖尿病的诊断。通常,正常人血清空腹血糖浓度为3.6mm到6.1mm之间。餐后血糖水平可能会升高,但通常小于10mm。如果血糖浓度超过11mm,这很可能预示是糖尿病患者。为了避免检测血清样本中葡萄糖浓度的限制,将1%胎牛血清(fbs)加入缓冲溶液中以模拟真实的血清环境,同时稀释葡萄糖浓度。结果如图12a(实心点)所示。与白点曲线(缓冲液)相比,实心点曲线(1%fbs)显示出几乎相同的测定范围(0-200μm)和相似的斜率(~0.04)。唯一的区别是实心点曲线存在较大截距,这意味着fbs含有一定量的葡萄糖。结果表明tpe-ipb具有良好的抗干扰能力,并且在血清环境中同样具有表现良好。这也证明了这种测定方法的可靠性。此外,还检测了不同糖类中tpe-ipb对葡萄糖的选择性。如图12b所示,在含有葡萄糖的探针溶液中观察到约15倍的pl增强,而其他糖如半乳糖,甘露糖,果糖,乳糖,蔗糖和葡聚糖等溶液中,仅引起微小的变化,这说明tpe-ipb对葡萄糖具有优异的选择性。
荧光检测onoo-
受到对不同ros类型的选择性检测的启发,tpe-ipb也可能响应于onoo-,因为onoo-可以诱导tpe-ipb荧光的显著增强。因此,研究了ph对tpe-ipb在h2o2和onoo-存在时的pl响应的影响。如图13所示,onoo-能在生理条件下(ph7.4)开启tpe-ipb的荧光,同时缓冲碱性可促进其裂解反应,导致更高的荧光增强。而h2o2只能在强碱性条件下(ph9.0-10.0)活化tpe-ipb。这个结果表明onoo-与tpe-ipb具有更高的反应活性。基于这个发现,tpe-ipb也可以用于onoo-的检测。因此,使用具有生物相容性的lipid-peg2000作为包封基质来包裹tpe-ipb,制备得到包裹了tpe-ipb的lipid-peg2000纳米探针(tpe-ipb纳米探针)。在纳米探针形成期间,疏水性脂质和tpe-ipb分子彼此缠结,所得聚集物成为纳米探针的核心。
另一方面,亲水性peg链被暴露于水相中成为亲水外壳,具有使纳米探针稳定的作用(图14a)。使用没有任何材料包裹的单纯tpe-ipb聚合体作为对照,图14b所示,在相同的荧光原浓度(40μm)条件下,pbs缓冲液中的tpe-ipb聚集体和tpe-ipb纳米探针的照片。pbs溶液中的单纯tpe-ipb聚集体呈现出蓝白色并且有点混浊。相比之下,tpe-ipb纳米探针更透明,表明lipid-peg基质可以帮助tpe-ipb更好地溶解在水溶液中。动态光散射(dls)结果显示tpe-ipb聚集体具有较宽的尺寸分布,在pbs缓冲液中粒径约377nm,而tpe-ipb纳米探针则具有更小的流体动力学直径,约34nm,和更窄的分布宽度(图14c)。通过透射电子显微镜(tem)研究tpe-ipb纳米探针的形态。如图14d所示,tpe-ipb纳米探针呈均匀球形,直径约30nm。此外,不同于tpe-ipb聚集体容易在pbs缓冲液中形成沉淀,tpe-ipb纳米探针表现出优异的胶体稳定性,如其稳定的尺寸分布所证明的,即使置于pbs缓冲液中2周后仍保持稳定。
随后研究了tpe-ipb纳米探针对ros的响应性。包括tbhp,clo-,·oh,roo·,o2·-,h2o2和onoo-在内的各种ros分别与tpe-ipb纳米探针在ph7.4的pbs缓冲液中的共同孵育。值得注意的是,只有onoo-可以引起纳米探针较大的荧光改变,而其它反应性氧氮物种(rons)几乎无的发光强度变化(图15a)。这个结果表明tpe-ipb纳米探针在生理ph条件下对onoo-检测具有高度选择性。图15b表示,在ph7.4的pbs缓冲液中加入不同量的onoo-后,tpe-ipb纳米探针的pl光谱图。随着onoo-浓度从100增加到400μm,纳米探针在538nm处的pl强度呈线性增强。与pbs缓冲液中纳米探针本身的发射相比,用400μmonoo-共孵育后的tpe-ipb纳米探针可观察到20倍的pl增强。该结果表明,onoo-能够以令人满意的信噪比开启tpe-ipb纳米探针荧光,并得到高发射性的tpe-iph纳米探针。
动力学研究还进一步通过在pbs缓冲液中将tpe-ipb纳米探针或tpe-ipb聚集体与onoo-(400μm)于37℃共孵育。图15c显示其最大pl强度的时间变化趋势。加入onoo-后,tpe-ipb纳米探针荧光显著地开启,并在20分钟时达到平台期,此时约有20倍pl增强。相反,tpe-ipb聚集体的pl强度超过40分钟才到达平台期,且仅提高了5倍。这个结果表面tpe-ipb纳米探针具有比单纯聚集体更快的onoo-响应速度和更高的荧光“开启”比率,这都归因于纳米探针较小的粒径和较大的比表面积。这也突出了使用lipid-peg基质的必要性和重要性。利用商业qd565和异硫氰酸荧光素(fitc)作为参照,对得到的发射型tpe-iph纳米探针的光稳定性进行评估。在连续10分钟激光扫描下监测纳米探针、qd565或fitc分别处理后的mcf-7癌细胞的荧光变化。如图15d所示,tpe-iph纳米探针在连续10分钟照射后仅出现约7%的pl强度损失,这与qd565(约5%损失)相当,但是比fitc(约53%损失)的稳定性更好。由于量子点以其强抗漂白性而闻名,这一结果表明该荧光纳米探针具有强的光稳定性。基于上述结果,可以得出合理结论:tpe-ipb纳米探针可以用作特异性检测onoo-的aie点亮型纳米探针。
特异性体内炎症成像
已知体内免疫细胞如巨噬细胞会迁移到炎症区域并活化同时释放大量的包括onoo-在内的rons。因此,在体内应用之前,先将tpe-ipb纳米探针用于检测巨噬细胞(raw264.7)产生的内源性onoo-。为了诱导胞内rons(如onoo-和clo-)的升高,巨噬细胞预先用细菌细胞壁脂多糖(lps)和佛波醇12-肉豆蔻酸酯13-乙酸酯(pma)处理。随后分别用tpe-ipb纳米探针与具有或不具有lps/pma刺激的巨噬细胞共孵育,随后用共焦激光扫描显微镜(clsm)进行细胞成像。未经lps/pma刺激的巨噬细胞表现出与背景荧光类似的荧光信号,而经过处理的巨噬细胞则表现出强烈的荧光信号,表明tpe-ipb纳米探针在炎症情况下的巨噬细胞中的可以显著地发光。此外,n-乙酰半胱氨酸(nac)被用来阻断lps/pma处理后的巨噬细胞中ros的产生。用nac清除rons后,与纳米探针共孵育的细胞中的荧光信号显著降低,证明荧光的“开启”根源于tpe-ipb纳米探针与细胞内源性产生的ros之间的特异性相互作用。
此外,评估了tpe-ipb纳米探针的体内毒性。将纳米探针于健康小鼠静脉注射,其浓度高于后续体内成像实验5倍。包括小鼠体重变化,血液化学测试以及重要器官(肝,脾和肾)组织学分析等数据显示tpe-ipb纳米探针的体内应用是相当安全的(图16)。
接下来检测了上述aie点亮型纳米探针在体内炎症成像的应用。由于血管的渗透性以及活化的免疫细胞会在炎症区域中生成大量的onoo-,tpe-ipb纳米探针将优先通过epr效应富集到炎性区域,炎症区域内升高的大量onoo-会显著的点亮纳米探针的荧光信号,从而实现对体内炎症的高选择性及强对比度成像(图17a)。
为了进一步验证这种纳米探针确实可以为体内炎症特异性成像提供新的机会,利用细菌感染诱导的炎症裸鼠作为模型动物,于小鼠左后部皮下接种耐甲氧西林的金黄色葡萄球菌(mrsa),制备小鼠炎症模型。通过组织学分析验证了该感染区域的炎症反应的激活。静脉注射tpe-ipb纳米探针后,通过maestroex体内成像系统对炎症的小鼠进行成像,并通过光谱去噪消除小鼠自发荧光。如图17b所示,纳米探针注射之前没有观察到可检测荧光信号,并且纳米探针给药后0.5小时,通过炎症区域与在其他组织中可忽略的荧光信号对比来明确炎症区域。炎症部位的荧光信号也随着时间的推移而增加,并在静脉注射tpe-ipb纳米探针3小时后荧光信号变得非常强烈。令人鼓舞的是,在纳米探针给药后,小鼠的其他组织中没有观察到可检测到的荧光信号。
aie点亮型纳米探针在炎症成像中的高选择性通过对不同组织离体成像来进一步证实(图17c)。通过对小鼠组织半定量研究表明,细菌感染皮肤中的平均荧光强度比其他组织高12倍(图17d)。众所周知,纳米材料容易被网状内皮系统(res)器官如肝脏和脾脏摄取。而tpe-ipb纳米探针注射后的小鼠res器官中的几乎可忽略的荧光信号表明aie点亮型纳米探针在正常组织中不会被点亮。这一结果表明,tpe-ipb纳米探针对高onoo-累积的体内炎症区域的可视化是高度特异性的。此外,进一步将感染和未感染的小鼠皮肤切片用于血管染色和clsm成像。如图17e所示,在细菌感染区域的血管周围能清楚地观察到黄色荧光点聚集。与此相反,在正常皮肤切片中几乎没有检测到纳米探针荧光信号。单细胞分辨率的这一结果证实了我们的纳米探针会在炎症区域点亮
可视化抗炎剂的体内治疗疗效
能够实现体内疗效可视化的抗炎剂新探针的设计对选择有效且可靠的抗炎药物具有临床价值。为了评估本申请中的aie点亮型纳米探针的能力,分别在裸鼠的左右背部皮下接种mrsa和大肠杆菌(e.coli)两种细菌,以建立炎症小鼠模型。将小鼠分成两组,分别使用不同的抗生素处理2周。第一组小鼠每天通过腹腔注射全身给予万古霉素。万古霉素是治疗由革兰氏阳性细菌例如mrsa引起的感染的重要抗生素。但大肠杆菌是一种典型的革兰氏阴性菌,对万古霉素耐药。另一方面,第二组小鼠使用对大肠杆菌菌株有效且敏感的抗生素-青霉素进行治疗,但青霉素对mrsa细菌感染无效。
在炎症形成后,抗生素治疗前,将tpe-ipb纳米探针静脉注射到两组小鼠体内。如图18a和18b所示,在治疗之前,两组小鼠的背部两侧(只在感染部位)可以清楚地观察到强烈的荧光信号。此外,分别在抗生素治疗7天和14天后,对两组小鼠进行aie点亮型纳米探针的静脉注射。可以观察到万古霉素治疗小鼠的mrsa感染病灶(图18a)的荧光信号以及青霉素治疗小鼠的大肠杆菌感染的病灶(图18b)的荧光信号随时间显著降低,并且在第14天几乎消失。相比之下,即使经过14天的治疗,细菌相应的注射抗生素耐受的炎性区域的荧光强度仍几乎保持不变。
在第14天,分别处死两个抗生素处理组的小鼠,收集所有细菌感染部位皮肤组织并切片,用于进一步分析。组织学检查揭示了万古霉素处理的大肠杆菌感染灶(图18c)和青霉素处理的mrsa感染灶(图18d)的苏木精和伊红(h&e)染色切片中的大量免疫细胞浸润,表现出典型的炎症反应特征。与此相反,从万古霉素处理的mrsa感染灶(图18c)和青霉素处理的大肠杆菌感染灶(图18d)的切片均能观察到得到了极大缓解的炎症以及几乎不存在细菌感染。此外,还发现在炎症区域血管周围有大量纳米探针荧光存在,而在有效抗生素治疗的区域中仅能探测到极少的纳米探针荧光(图18e和18f)。该结果与图18a及18b中的非侵入性数据结果一致。结果不仅验证了本研究中使用的抗生素的良好选择性和高治疗效果,而且还证明了该aie点亮型纳米探针可为抗炎剂体内治疗效果提供非侵入的和实时的信息。
用于细胞器靶向的红色荧光aie分子
本专利材料有关于几组红色荧光aie分子及其生物应用。并且,用于细胞器特异性成像的靶向部分都连接在这些分子上。
合成及一般性质
化合物6(a-c)的合成路线图如下:
化合物12的合成路线图如下:
化合物16和17的合成路线图如下:
我们的合成路线基于科诺瓦诺格缩合反应和铃木偶联反应。产物通过核磁谱以及质谱表征,分析数据皆与给定的分子结构完美相符。
化合物6(a-c)和12在不同溶剂下的吸收峰区域在450nm左右,其在不同溶液中的荧光在600nm到650nm的范围中(图19-22)。这是典型的分子间扭曲分子内电荷转移(tict)现象,也就是非极性溶剂会使荧光信号增强且蓝移,极性溶剂会使荧光信号减弱且红移。此处,dmso与甲苯混合溶剂用于aie性质探究,dmso用作良溶剂而甲苯用作不良溶剂。在纯dmso溶剂中没有荧光发射,但随着甲苯含量在dmso溶液中的增加,荧光信号得到增强且出现蓝移。当甲苯含量在甲苯/dmso混合溶液中低于80%时,荧光信号因为不良溶剂引发tict效应而增强。而甲苯含量高于80%时,荧光信号因aie性质而急剧增加。一旦聚集态形成,分子内运动受限,能量得以通过荧光辐射跃迁而不是非辐射跃迁。对于化合物16以及17,吸收光谱分别在410和525nm(图27-28).化合物16具有aee效应,在600nm左右的荧光发射随着水含量增加而增强且红移。对于化合物17,在650nm左右的荧光发射得到增强,但在50%水含量下会减弱(图30),此现象可能由于分子间距离太近导致pi-pi相互作用而造成。
化合物6a的应用
细胞定位性质
由于其光谱吸收在可见光区域,荧光对极性感应灵敏。而线粒体靶向基团可用作细胞成像探针。海拉细胞被置于含有化合物6a(5μm)的培养基中培养30分钟。意外地,荧光成像中出现了两种颜色,分别是线粒体中的橙色与细胞核中出乎意料的红色。首先,我们确认了线粒体特异性。海拉细胞与化合物6a以及线粒体追踪子共染的共焦成像显示了他们荧光信号的定位重叠。为了分开两种细胞器的荧光信号,我们使用共焦成像检测,并收集从500到750nm的发射信号。405nm以及560nm两段不同波长用作激发。在405nm激发下,只在线粒体里出现信号;而在605nm激发下,细胞核中也出现了信号。基于在细胞成像中,单一探针在不同激发波长下产生双色光以及不同选择性的发现,我们推导两种不同荧光颜色有可能是由于它们在细胞核以及线粒体的不同作用。
线粒体膜中最主要及最大量的成分是磷脂,而在dna和rna中,磷脂主要富集中在细胞核中。为了模拟细胞环境,我们将不同种类的磷脂,dna以及rna溶液与化合物6a溶液混合配置。
化合物6a与磷脂混合物的最高吸收峰在430nm,而在加入dna或rna后出现了30nm的红移(图31a)。在磷脂和dna或rna混合溶液中,发射光谱也同样出现由600到680nm的红移(图31b)。实验结果表明细胞成像中呈现的两种颜色是由于不同相互作用造成;同样地,也表明了线粒体特定在405nm激发下成像而细胞核特定在560nm激发下成像,这是因为在磷脂和dna或rna溶液中的吸收的不同。405nm的激发光源能更多地被含磷脂溶液吸收而非dna或rna溶液,而560nm的激发光则大部分被含dna或rna溶液吸收而非磷脂溶液。
化合物6a与线粒体中磷脂的作用应该为静电作用。在磷脂溶液中,吸收峰没有产生位移,而最强的吸收来自在带两个负电荷的tocl溶液中。有人提出化合物6a与rna或dna的相互作用是静电吸引及插层,因为dna和rna存在磷酸基团,同样带负电荷。化合物6a带一个正电荷,能被dna或rna吸引。但在接近之后,化合物6a有可能扩散并滑入dna或rna的疏水环境中。该现象可通过dna或rna的吸收红移来解释,意味着化合物6a变得更加共平面。荧光光谱也因为增加的共平面结构而红移。此外,其他可能性包括插层位点可能仍在极性环境中,因为主链中的碱基对有氢键相互作用,其中的tict效应使得发射也更加红移;而这发射的红移现象可能是由于在电插层点处形成了d-a配合物。
细胞核特异性的机理
细胞核中含有大量的蛋白质及rna,如核糖体蛋白和rrna。为了进一步了解化合物6a在细胞核中的相互作用,我们在固定的细胞中进行核糖核酸酶(rnase)和脱氧核糖核酸酶(dnase)的消化测试,并以sytornaselect作为对照。经过rnase处理后,细胞核中的信号明显消失,而在dnase中信号保持不变。这是证明细胞核中大部分信号来自于ascp和rna的相互作用的直接证据。
为了模拟消化测试,我们研究了pl光谱的变化(图32)。有趣的是,由于dnase和rnase的消化不同,荧光信号只在rnase处理中显着降低。我们的是使用dnasei和rnasei,其能将单链和双链dna消化成含有5'磷酸的寡脱氧核糖核苷酸;其降解所有rna二核苷酸键,留下5'羟基和2',3'环状单磷酸酯。虽然经过dnase处理,但dna在ascp仍有相互作用的位置只能被切成小片。
如图48a所示,与dna相互作用的位置有荧光现象,但细胞成像中的红色与dna无关,而是因为购买的用于实验的dna的不同以及细胞中的dna也不同。细胞dna由组蛋白包装和排序,但在体外dna中并没有组蛋白。组蛋白携带部分正电荷,可与dna相互作用。使得dna中的正电荷可能被中和,然后对化合物6a的吸引力降低。
信号分析,光稳定性与细胞毒性
来自线粒体和细胞核的荧光信号有部分重叠,即使在560nm激发下,我们也尝试通过收集650-750nm的信号范围来使来自线粒体的信号最小化从而强调不同的荧光细胞核。该方法成功得到具有更高的对比度荧光细胞核(图33a)。同时,将化合物6a与sytornaselect在共焦成像中进行比较。光稳定性对于监测线粒体和核仁形态变化以及研究这些过程和关系十分重要。在560nm激发光的连续扫描下,化合物6a的信号在第50次扫描中仍几乎保持在98%以上,但在第15次扫描中sytornaselect的信号几乎到0%左右了(图33b)。细胞核的形态仍然清晰可分辨,但sytornaselect的荧光信号则消失了。
我们通过mtt法测定在hela细胞中测试化合物6a的细胞毒性(图34)。结果表明,不同染料浓度下细胞存活率均在90%以上,证明了化合物6a的生物相容性。由于化合物6a仅在30分钟内与细胞培养,因此可认为是无毒的。考虑到细胞核和线粒体改变的研究,化合物6a符合强光稳定性,生物相容性以及高特异性的要求。重要的是,信号可以分开研究,并且可以在不同的荧光颜色下观察。化合物6a具有很高的监测核仁和线粒体变化和关系的可能性。
6b,6c及12的应用
将化合物6b用作线粒体靶向染料,将化合物6c和12用于细胞膜靶向。化合物6c和12带正电荷,具有相比于化合物6b更长的疏水部分。它们可以在细胞膜的双层脂质中被追踪检测。然而,我们发现化合物6b和6c可用于双光子成像,可以在uv照射下产生ros。它们也可以用于影相导航的光动力治疗。因此可能有助于研究细胞凋亡和坏死过程。
辐射增敏作用
为了研究6b的氧化作用,将a549癌细胞与ascp-2p培养2小时。然后,将ros检测器dcfh加入介质中,随后暴露于白光(25mwcm-2)1分钟。之后,立即在clsm下观察这些细胞。如图8d-f所示,绿色荧光代表细胞内ros的水平。绿色荧光越亮,细胞内ros水平越高。值得注意的是,如较亮的荧光所代表的,6b可以显着增加细胞内ros的水平,这表明光是6b诱导ros产生的有效触发出器(图43e)。此外,抗氧化剂n-乙酰半胱氨酸(nac)与6b的共处理实质上逆转了ros的诱导,证明了通过光对6b的ros诱导作用可被抗氧化剂nac消除(图43f)。
我们采用xtt法来评估6b的抗癌作用。如图43g所示,没有光照情况下6b对a549细胞几乎无毒性。即使在最高浓度(80μm)下也有近90%的细胞存活。然而,当暴露于白光1分钟,6b导致与剂量相关的细胞死亡。ic50值约为33μm。另外,与nac的共处理显著减弱了6b在光照下的细胞毒性作用。例如,80μm的6b导致超过90%的细胞死亡,而在nac共处理时超过75%的细胞存活。
我们通过进行克隆形成试验来评估6b的放射增敏作用。照射前,将a549癌细胞与6b(5μm)培养2小时以确保6b靶向递送至线粒体。之后,以一系列剂量(2,4,6gy)进行照射。然后立即将细胞接种到6孔板中以研究克隆形成能力。如图44a和44b所示,与单独光照相比,无光照下的6b没有显示出放射增敏作用。然而,6b处理的细胞暴露于光照后明显地使癌细胞对辐射敏感。ser10计算值为1.62。
最近的研究表明,某些药物具有放射增敏作用,如紫杉醇,顺铂等。临床研究还表明,紫杉醇已被推荐为同步化疗/放疗的标准疗法。另外,一些研究集中在可能具有放射增敏作用的潜在纳米材料上。金纳米粒子(gnp)是纳米技术领域中最有前景的放射增敏剂之一,因此我们把6b与紫杉醇和gnp的放射增敏作用作比较。图44c和44d显示,在光照下6b是能够使肺癌细胞对辐射敏感的最有效的药剂。6b和紫杉醇或gnp处理的细胞的集落形成能力有显着差异。从曲线计算,紫杉醇的ser10为1.32,而gnp的ser10为1.19。两者均明显低于6b的ser10,达到了三种药物中最高的1.62。
为了研究放射增敏作用的潜在机制,我们选择较低剂量的6b(5μm)与辐射组合。5μm的6b在光照下诱导很少的细胞凋亡,可以认为是几乎无毒。如图45a所示,单独照射抑制akt和erk的磷酸化,而在光照下的6b则几乎不影响p-akt和p-erk的表达。更重要的是,6b与光和辐射的组合明显阻断了磷酸化过程,表明对p-akt和p-erk抑制的协同作用。此外,我们还通过western印迹评估了下游凋亡途径(图45b)。在光照下6a诱导极少的细胞凋亡,而辐射则抑制了(bcl-2,bcl-xl)的表达,促进促凋亡蛋白(bax,bad)的表达。其中一个最重要的凋亡标记物(caspase-3),出现了(caspase-3)的减少以及(cleavedcaspase-3)的增加。而且,辐射与6b组合在光照下比单独辐射或单独6b光照更有效地诱导细胞凋亡。
另外,使用抗氧化剂nac作为ros清除剂来研究6b的放射增敏作用是否主要依赖于细胞内ros的诱导。显然,nac显着减弱了6b对p-akt和p-erk表达的抑制作用,逆转了对下游凋亡途径的诱导。例如,与nac的共处理在6a暴露在光照下后,基本上降低了抗细胞凋亡bcl-2的表达,并加强了促凋亡蛋白bax和bad的表达,这清楚表明了6b的放射增敏效果与与光诱导细胞内ros密切相关。已知癌细胞对辐射的抵抗与pi3k/akt和mapk通路的调控密切相关。同时,一些研究表明,保护细胞免于细胞凋亡的pi3k/akt的组成性表达,在癌细胞的化学增敏中起关键作用。6b的有效ros诱导作用是由光照引发的,它可以通过抑制p-akt和p-erk以及随后的细胞凋亡诱导而用作对辐照的有效放射增敏剂(图45c)。
质膜的形态变化
程序性细胞死亡称为细胞凋亡,由外因引起的死亡称为坏死。细胞凋亡或坏死时膜的形态会发生改变。质膜的形态变化与细胞的健康有关。但是,动态变化很少被记录下来。由于染料可选择性靶向质膜,且具有较高的光稳定性和较高的生物相容性,因此可用于质膜的长期跟踪。
汞是对人类和动物毒性最大的元素之一。hg2+可引起细胞功能障碍,诱导细胞死亡。华等已经报道了hg2+离子会改变膜的形态并诱导水泡形成,这是细胞死亡的常见征兆。12用于监测hg2+处理下hela细胞的动态变化。在图43中,假彩和假绿色分别代表hg2+处理前后。我们发现质膜出现变化。处理40分钟后形成水泡。水泡形成意味着hg2+与细胞骨架有相互作用(图46a),导致肌动蛋白丝破裂。当肌动蛋白丝被破坏时,被破裂位中的液体静压力增加并迫使双层膜渗出。为了确认气泡形成不是由染料引起,我们进行了对照实验,发现质膜的形态不会发生很大变化。证明了在毒性条件下通过12监测质膜形态变化的可能性。
细胞粘附是必不可少的,并广泛用于生物学实验。它是细胞与表面,底物或其他细胞相互作用和附着的过程。这些相互作用是由跨膜糖蛋白(称为细胞粘附分子(cam))的作用驱动的。cam是细胞表面上的蛋白质,并与细胞外基质结合。选择蛋白,整联蛋白,syndecans和钙粘蛋白都是cam的特例。在盖玻片上粘附的过程中,细胞的形态在盖玻片表面由球形变为扁平状。这个过程被充分研究,进而假设出粘附的关键步骤。贴壁细胞可以被能够切割肽键的胰蛋白酶分离。当cam被胰蛋白酶消化后,贴壁细胞将离开表面,扁平形状恢复为球形(图47)。12可用于监测贴壁细胞脱落的过程。
首先,使用共焦显微镜作贴壁细胞成像(图48a)。加入胰蛋白酶后,在不同时间记录图像(图48b-h)。细胞的外观变成更小的球体,这意味着细胞正从盖玻片上离开。但更有趣的是,7分钟后可观察到细胞周围的一些小球体。这是首先使用荧光技术观察到的现象。我们提出在分离过程中双层膜会发生解离。当添加了胰蛋白酶并开始消化cam时,细胞开始因表面上缺乏足够的结合点而脱离。这意味着即使细胞正在脱离,一些cam仍然没有被消化。在结合点处,质膜被强制脱离,但cam将膜保留在盖玻片上。结果,在这种拉动下,一些膜可能从细胞中裂解。由于膜是双层磷脂,裂解的膜倾向于形成微团。本染料在双层中被追踪。我们可以通过观察细胞的形状来监测分离的过程。另一方面,我们还可以详细地监测一些像微团形成的微小过程。结果表明,12是长效监测质膜形态变化的潜在候选药剂。
质膜中的ros诱导变化
在证实6c可以在体外产生ros之后,我们尝试确认水泡的形成与ros有关。6c和h2dcfda在hela细胞中共染并记录其相应的信号(图49)。在405nm激发光照射4分钟后,来自ros传感器的信号逐渐开启并变得高发射,意味着ros在照射下产生。同时,发现6c的信号从质膜进入细胞。这可能意味着膜的刚性在照射过程中发生了变化。染料不能紧密跟踪,然后扩散到里面。
考虑到光照射期间的刚性,我们尝试使用pi研究质膜刚性破坏后的渗透性。pi不能进入活细胞,但由于质膜的通透性可进入死细胞。当它进入细胞时,它与dna相互作用并以红色发射点亮。用6c染hela细胞后,将pi引入细胞培养物中。在照射前,没有发现来自pi的红色荧光信号,但有信号来自膜中的本染料(图50)。在照射下,荧光并逐渐增强,这意味着pi正在进入细胞并与dna相互作用。收集增加的信号以实时监测pi的点亮过程(图51)。重要的是,这个结果意味着质膜的渗透性在照射后减弱或消失。ros没有破坏f-肌动蛋白皮层以及质膜的磷脂。
生物相容性
在研究了6c的性质之后,显示出其有可能成为pdt的光敏剂。使用mtt法来研究这个想法的可能性(图52)。pdt需要一种无毒的药剂,并且该药剂可以产生类似于ros的毒素以杀死细胞。6c在黑暗条件下或无光照条件下具有较好的生物相容性,因细胞存活率较高,且细胞存活百分率在光照条件下急剧下降。这个光控过程结合6c的荧光可以进一步发展为影相引导的pdt。
16和17的应用
化合物16被用做溶酶体靶向。选择性由商业染料,溶酶体红色荧光探针确定。它也可以用于双光子成像,以提供更高的分辨率和更高的信噪比。化合物17用于脂滴成像。在共焦图像中,信号来自整个细胞。然而,当发射收集范围从520nm变为630nm时,由脂滴的非极性环境,信号仅来自脂滴,这将使化合物17的发射转移到更蓝的区域中。
在实施方案中,本专利材料针对在uv照射下产生和/或跟踪活性氧物质(ros)的探针,其包含具有以下结构的红色荧光aie分子:
在实施案例中,本专利材料的探针是一种染料。
在实施方案中,本专利材料针对用于监测质膜的长期形态变化的探针,并具有以下结构的红色荧光的aie分子:
在实施方案中,本专利材料的探针可提供细胞膜染色。
近红外发光aie分子的生物应用
合成方法与性质
一系列目标化合物是以tpe-tetrad为分子骨架,tpe-etrad具有近红外发光,大的斯托克斯位移,低细胞毒性,高光稳定性。这些良好的aie和tict性质使得有可能利用这种染料协同作用于各种多功能纳米颗粒平台。用聚乙二醇聚合物、多孔二氧化硅和生物分子基质封装近红外发光的aie纳米聚集物发射器可以制备出高亮度、低细胞毒性的均匀尺寸的纳米颗粒。与之相关的应用包括生物成像,长期的细胞追踪和有机发光二极管(oled)。
用于合成这类独特的红外发射器的合成方法是基于成熟的knoevenagel缩合反应和铃木偶联反应。tpe-tetrad(化合物6)详细的合成路线如下所示:
光学性质
根据已建立的结构设计原理,aie激活发光的成分是共价键合到常规的荧光基团来赋予他们aie性质,四个tpe单元结合到具有tpa-dcm的分子框架。整体的结构显示有aie和tict的性质。tpe-tetrad在thf里具有最大发射波长为668nm,和tpa-dcm相比有53nm红移。
通过逐渐增加水的含量,tpe-tetrad发光强度急剧减弱并且出现了发光红移的现象,这是因为溶剂极性增加和tict产生的构相转变。荧光发射在水的含量≈50%时有所体现并且随着含水量增加进一步增强。同时,当含水量到90%时发射最大值逐渐红移至675nm。这些数据证实了tpe-tetrad是具有tict和aie双重特性的发光分子。509nm处的最大发射吸收产生了相对大的160nmd斯托克斯位移。
用tpe-tetrad从固体到纳米粒子的各种状态下得到的各种量子产率和寿命在表1中概述。
表1:不同tetrad的量子产率和寿命
最值得注意的是,固体状态的发射高达23.41%,寿命为3.55ns。双光子截面在803nm为313g,使得这种染料在深层组织成像和生物应用非常有用。这可以看出,tpe-tetrad在800nm处的在双光子激发发射光谱中与生物窗口有显著的重叠。
纳米颗粒的制备及生物应用
为了进一步探究tpe-tetrad在生物上的应用,我们研究了三种不同的纳米颗粒。第一种也是最基本的方法涉及到使用dspe-peg2000封装tetrad染料。通过分散tpe-tetrad在thf中然后慢慢加入dspe-peg2000的水溶液得到。随后,该tpe-tetrad分子聚集并和dspe-peg2000疏水部分相连。超声处理后立即形成稳定的纳米颗粒。除去thf然后通过一个0.45μm微型过滤器纯化。纯化的纳米颗粒的负分zeta电位表明这些纳米颗粒由于外层的离子化羧基而稳定。动态光散射证实纳米颗粒的粒径为230nm。
正如mtt所表明,这种纳米颗粒显示出很低的细胞毒性。此外,这种高共轭分子表现出ros的能力。这非常不利于长期细胞跟踪研究,因为长期的共聚焦显微镜激光曝光带来的无意识细胞毒性。tpe-tetrad染料和纳米粒子无法产生大量的ros。然而,这种tpe-tetrad纳米粒子能够hela细胞内化,显示出非常明亮的荧光。
研究的下一个纳米粒子系统涉及在tpe-tetrad纳米颗粒外包裹多孔硅的涂层,使粒子具有优异的长期稳定性和多功能的药物释放能力。如mtt法所示,观察到的细胞毒性非常低,有高于95%细胞存活率。第三个也是最后一个研究的纳米颗粒平台是把金纳米颗粒(aunp)引入到前文提到的tpe-tetrad和peg基质中。
在一个实例中,本专利涉及一种近红外aie探针:
在一个实例中,本课题的探针用于深层组织成像。在实例中,本课题的探针用于药物递送。在一个实例中,本课题的探针被hela细胞内化。
tpe-py-ffgysa和tpe-py-ysa的制备与表征
一种异硫氰酸酯官能化的aie发光分子,即tpe-py-ncs,被合成并且通过标准的光谱技术进行了表征。tpe-py-ffgysa和tpe-py-ysa的合成路线如下图所示:
通过标准的固相肽合成法合成了nh2-ffgysa肽,并通过液相色谱(lc)、1hnmr和hrms进行表征。tpe-py-ncs的异硫氰酸酯基和nh2-ffgysa胺基反应生成tpe-py-ffgysa,产率70%。最终化合物的纯度和化学结构通过lc、1hnmr和hrms证实。作为对照,没有ffg序列的tpe-py-ysa和tpe-py-ffgysa合成和表征方法相同。
光学性质
tpe-py-ncs的aie性质通过测试在四氢呋喃/正己烷的pl光谱得到证实。如图53a和53b所示,tpe-py-ncs在纯四氢呋喃溶液中,在626nm处显示出相对较弱的发射峰。随着四氢呋喃/正己烷混合物中正己烷含量的增加,从0到70%,pl强度略有提高,发射波长明显蓝移。这种现象应归因于典型的tict影响:当正己烷含量上升,混合溶剂极性增大。随着混合溶剂中正己烷含量进一步增加,导致了在595nm处荧光急剧增强,说明了aie效应。
pe-py-ncs。tpe-py-ffgysa和tpe-py-ysa在pbs的发射光谱分别如图53c所示。tpe-py-ffgysa和tpe-py-ysa在pbs缓冲剂里都发出微弱的荧光,尽管tpe-py-ffgysa的荧光强度是tpe-py-ysa的2.2倍。值得注意的是,当分别置于纯水、pbs缓冲剂、dmem培养基、含胎牛血清dmem中,tpe-py-ffgysa和tpe-py-ysa的pl光谱几乎没有变化。这表明了tpe-py-ffgysa和tpe-py-ysa可以作为适用于复杂生物环境的turn-on型荧光探针。
pc-3肿瘤细胞特异性成像
据报道,epha2蛋白在人前列腺癌pc-3肿瘤细胞中高度表达,并通过pc-3细胞和商业单克隆抗epha2蛋白抗体和随后的荧光二级抗体的染色实验证实(图54)。因此,pc-3细胞裂解液分别用于tpe-py-ffgysa和tpe-py-ysa,紧接着pl测试。正如图53c所示,一加入pc-3细胞裂解液,tpe-py-ffgysa和tpe-py-ysa在575nm的发射峰大大增强。值得注意的是,pc-3细胞裂解液处理后,和tpe-py-ysa的荧光强度比,tpe-py-ffgysa高了3.7倍,表明tpe-py-ffgysa有较大的荧光信号输出。
实验研究了是否该治疗诊断剂可以以选择性和高对比的方式对在癌细胞中过表达的epha2蛋白进行成像。在这个实验中,pc3肿瘤细胞和人平滑肌细胞分别作为epha2阳性和阴性细胞。通过抗体染色实验,验证了平滑肌细胞表达很少的epha2蛋白(图54),试验表明,正常细胞可以作为一个良好epha2阴性对照。需要注意的是,大多数epha2受体作为二聚体存在于癌细胞膜;然而,与特异性配体相互作用后(即抗epha2蛋白的抗体或ysa肽),epha2的二聚体容易在膜上组装成更大的团簇,接着是通过内化进入细胞浆。
tpe-py-ffgysa(1μm)用于培养pc-3肿瘤细胞。在37℃孵育90min,pc-3肿瘤细胞通过激光共聚焦扫描显微镜(clsm)成像。如图55a所示,在pc-3细胞的细胞核周围可以清楚的观察到亮黄色荧光的点,表明tpe-py-ffgysa的荧光可以在癌细胞中显著打开。为了验证tpe-py-ffgysa可视化的确实是epha2团簇,pc-3细胞与单克隆抗epha2蛋白抗体和荧光二级抗体进行了共染。发现tpe-py-ffgysa的黄色荧光(图55a)和抗体的红色荧光(图55b)在细胞里共存的很好(图55c)。由于抗epha2蛋白的抗体可以和epha2的特异性结合,上述结果合理地证明了tpe-py-ffgysa能够靶向并且照亮pc-3肿瘤细胞中的epha2团簇。此外,pc-3细胞在无ysa肽的环境下预处理随后在37℃加入tpe-py-ffgysa培养90分钟。clsm图像如图56示,一旦阻断epha2受体,pc-3细胞中的荧光信号明显降低。这一结果表明,tpe-py-ffgysa的荧光来源于与epha2受体特异性结合。
为了测试tpe-py-ffgysa跟踪epha2胞内运动的可行性,pc-3肿瘤细胞首先在0℃和tpe-py-ffgysa培养,因为蛋白的内化具有能量依赖性。在0℃培养1h后,pc-3肿瘤细胞的细胞膜上观察到tpe-py-ffgysa的强烈的荧光信号(图55d),表明了epha2受体起初是分布在细胞膜上。另外,在0℃处理tpe-py-ffgysa1小时后,洗涤pc-3细胞并且在培养基中再培养10和60分钟,然后用激光共聚焦显微镜进行活细胞成像。在37℃条件下进一步孵育10分钟,很明显黄色荧光信号可以定位于细胞膜和细胞质(图55e),这表明细胞在37℃更生时发生epha2受体内化。引人注目的是,在37℃进一步细胞培养60分钟后的细胞质中观察到绝大多数荧光斑(图55f),表明epha2集群几乎完全内化到pc-3肿瘤细胞。这一结果表明,tpe-py-ffgysa可以监测在活pc3肿瘤细胞中的epha2的细胞内运动。
除此之外,用epha2阴性平滑肌细胞作为对照,来研究tpe-py-ffgysa的靶向能力和对epha2的特异性荧光开关。如图57a所示,一旦37℃下和tpe-py-ffgysa(1μm)培养90分钟后,在平滑肌细胞中检测到的荧光信号很少,表明tpe-py-ffgysa对照明在癌细胞中高度表达的epha2具有很高的特异性。除此之外,没有ffg序列的tpe-py-ysa被用作对照探针。图57b和图57c展示了pc-3肿瘤细胞分别和tpe-py-ffgysa(1μm)与tpe-py-ysa(1μm)37℃下培养90分钟后的clsm图像。和tpe-py-ffgysa处理的细胞相比,观察到tpe-py-ysa处理的细胞具有更少的微弱的荧光的不染区。图像增强软件的定量分析表明,tpe-py-ffgysa处理的细胞的平均荧光强度高于tpe-py-ysa处理的pc-3细胞4倍,这与细胞裂解液滴定数据吻合(图53c)。对比实验表明,相比tpe-py-ysa,tpe-py-ffgysa能够在癌细胞中更敏感和更高对比度的可视化epha2蛋白。另外,平滑肌细胞与tpe-py-ysa在37℃孵育90分钟后的clsm图像在正常细胞中传达非常弱的荧光信号(图57d),这与tpe-py-ffgysa-处理的平滑肌细胞(图57a)的荧光斑块数量和荧光强度几乎没有差异。
和tpe-py-ysa相比,epha2成像的tpe-py-ffgysa较大的荧光信号吞吐量在pc-3癌细胞应归因于aie分子和ysa之间的ffg序列。epha2作为受体会在癌细胞中形成集群,由于蛋白质和ysa的特异性结合,大量探针将显著富集于epha2集群。在蛋白质集群的表面,与tpe-py-ysa相比,可以设想在ff的作用下,tpe-py-ffgysa会形成更多、更紧密的含tpe-py的聚集体当用芳香族基团封端时它具有优异的自组装性,从而更有效地限制tpe-py苯环的分子内旋转,从而导致更高的荧光信号输出。结果,tpe-py-ffgysa通过简单地掺入三种氨基酸ffg,可以以更灵敏和更高对比度的方式使癌细胞中的epha2集群成像。
紫杉醇抗肿瘤作用的辅助扩增
其次,作为aie佐剂的先决条件,研究了tpe-py-ffgysa在光照射下产生ros的能力。在此实验中,使用2',7'-二氯二氢荧光素二乙酸酯(dcf-da)作为ros指示剂,它不发光,但在ros的存在下可以快速氧化反应变成荧光二氯荧光素(dcf)。如图58a所示,当tpe-py-ffgysa水溶液连续暴露于白光照射时,发现产生了有效的ros,在530nm处峰值荧光强度的显著增加。添加维生素c以清除生成的ros时,可以有效地抑制这种荧光增强指示剂。通过监测在418nm处dpbf吸光度的降低(图58b),另一个ros指示剂1,3-二苯基异苯并呋喃(dpbf)进一步证实了tpe-py-ffgysa产生ros能力。
同时还使用dcf-da作为指标评估在pc-3癌细胞中tpe-py-ffgysaros产生。与tpe-py-ffgysa(1μm)在37℃孵育90分钟后,pc-3细胞暴露于光照2分钟。如图58c所示,在光照射下,在tpe-py-ffgysa处理的细胞内可清楚地看到dcf的强烈的绿光发射。然而,在用n-乙酰半胱氨酸(nac)(一种ros清除剂)预处理细胞后,光照射下的tpe-py-ffgysa处理的细胞中dcf的荧光强度大大降低。这些结果表明,tpe-py-ffgysa生成的有效的ros可以靶向pc-3癌细胞中的epha2簇。相比之下,没有暴露于光照的tpe-py-ffgysa处理的细胞显示出与对照细胞类似的绿色荧光(图58c),表明光照射对于tpe-py-ffgysa产生ros是必需的。
采用mtt法研究tpe-py-ffgysa作为aie佐剂来增强ptx细胞毒性的作用应。tpe-py-ffgysa产生的外源性ros不会杀死癌细胞,而是提供了细胞内氧化环境来增强ptx的抗肿瘤效力。用tpe-py-ffgysa本身(1μm),“tpe-py-ffgysa(1μm)+光照射”或纯光照射处理后的pc-3癌细胞和平滑肌细胞的48小时生存力都高于95%(图59a),表明通过优化实验条件,即使暴露于光照下,tpe-py-ffgysa对癌细胞和正常细胞均无毒性。这个结果揭示了tpe-py-ffgysa有希望作为具有非常低的细胞毒性的佐剂。进行的光照射会导致tpe-py-ffgysa的协同抗肿瘤作用,接下来来研究ptx。
与tpe-py-ffgysa在37℃孵育90分钟后,洗涤pc-3癌细胞并暴露于32nm的ptx。随后,加入ptx后在0,3,6,9或12小时进行白光(0.1wcm-2,2min)的单次照射,然后在24小时进行mtt测定。如图59b所示,在ptx添加后0,3或6小时的光照射下,pc-3细胞存活率与没有光照(probe+;light-)的存活率没有显著差异。令人鼓舞的是,当加入ptx后12小时进行光照时,发现ptx的细胞毒性显着增强。这个结果意味着pc-3细胞与ptx相互作用12小时后,分子内氧化环境对于药物的更好作用很重要。
此外,在用一系列剂量的ptx孵育tpe-py-ffgysa处理的pc-3细胞后,在ptx加入后分别进行12,24和36小时3次光照射(0.1wcm-2)。每次照射持续2分钟。没有py-ffgysa处理有光照(probe-;light+)和没有光照有tpe-py-ffgysa处理(probe+;light-)对ptx的细胞毒性的干扰可以忽略不计。值得注意的是,“tpe-py-ffgysa+光照”(probe+;light+)的处理使得ptx的抗肿瘤功效显著增强。
如图59c计算的细胞毒性曲线所示,单独的ptx(probe-;light-)ic50值是75.9nm;当ptx与“tpe-py-ffgysa+光照射”结合时,ic50值显著降低到7.8nm,这仅是原始ic50值的10.3%。先前的研究报道,氨磷汀作为化学增敏剂可以将ic50值降低至单独ptx的14%,这是被公认的ptx抗肿瘤效力提高的优异表现。同时,强调“tpe-py-ffgysa+光”不能导致细胞死亡(图59a)是很重要的。因此,有理由推断在光照作用下tpe-py-ffgysa可以作为“0+1>1”效应的一种非常有效的与ptx协同抗肿瘤治疗的佐剂。
机理研究
通过蛋白质印迹检测相关蛋白的表达,来研究ptx和“tpe-py-ffgysa+光照射”之间的这种协同抗肿瘤作用的可能机制。如图60a所示,在没有ptx的情况下,与未处理的细胞相比(ptx-;probe-;light-),“tpe-py-ffgysa+光照射”(ptx-;probe+;light+)几乎不影响pc-3癌细胞中的蛋白质表达。这个结果证实“tpe-py-ffgysa+光照射”确实不会导致pc-3细胞的死亡。此外,用ptx单独处理的pc-3细胞(ptx+;probe-;light-)和“没有光照的ptx+tpe-py-ffgysa”(ptx+;probe+;light-)的蛋白质表达几乎没有差别,这进一步证实了光照是启动协同效应的关键因素。
值得注意的是,当与单独的ptx比较时,ptx和“tpe-py-ffgysa+光照射”(ptx+;probe+;light+)的结合使得磷酸化的akt(p-akt)的表达被更显着地抑制(图60a)。由于p-akt是癌细胞中非常重要的生存信号,早期的研究已经证明,p-akt的组成性表达破坏了癌细胞对ptx的敏感性。因此,在本研究中证明,抑制akt蛋白的磷酸化对“tpe-py-ffgysa+光照”在ptx的化学敏化起关键作用。
此外,还通过western印迹评估下游凋亡途径。很明显,与其他四个对照治疗相比,通过增加细胞色素c的细胞质表达和降低抗凋亡蛋白bcl-2的表达,ptx和“tpe-py-ffgysa+光照射”的结合更有效地诱导线粒体来源的细胞凋亡。此外,最重要的细胞凋亡标志物之一caspase-3的表达在组合治疗下经受最多的减毒(图60a)。此外,nac作为抗氧化剂的存在能够显著地消除协同抗肿瘤效力(图60b)。因此,这些结果共同阐明了潜在的协同机制,即由“tpe-py-ffgysa+光照射”引起的细胞内ros水平升高,从而通过增强对p-akt的抑制来放大ptx的作用,从而更有效地诱导线粒体起源细胞凋亡(图60c)。
在一个实施方案中,本主题涉及用于细胞器靶向的探针,选自以下的红色荧光aie分子:
在一个实施方案中,本课题的探针用于对pc-3癌细胞进行成像。在一个实施方案中,本课题的探针用于产生ros。在一个实施方案中,本课题的探针用作紫杉醇抗肿瘤治疗的佐剂。
例子
化合物3的合成
在100ml的圆底烧瓶中,将4-溴苯基乙腈(0.69g,3.50mmol)和化合物2(3.00mmol)溶解在40ml乙醇中并搅拌。在5ml乙醇中加入氢氧化钠(0.14g,3.50mmol),滴加到混合物中。2小时后,形成沉淀,过滤除去溶液,得到淡黄色固体,产率80%。
化合物3a:1hnmr(400mhz,cdcl3,·δ(ppm)):7.86(d,2h,j=8.4hz),7.54-7.48(m,4h),7.38(s,1h),6.73(d,2h,j=8hz),3.07(s,6h).hrms(maldi-tof)m/z326.0417(m+,calcd.326.0419).
化合物3b:1hnmr(400mhz,cdcl3,·δ(ppm)):7.97(d,1h,j=8.4hz),7.69(d,1h,j=8.0hz),7.58-7.47(m,6h),7.43(s,1h),7.38-7.27(m,4h),7.22(d,1h,j=8.0hz),7.16-7.12(m,4h),7.07(d,2h,j=4.4hz).hrms(maldi-tof)m/z450.0778(m+,calcd.450.0732).
化合物3c:1hnmr(400mhz,cdcl3,·δ(ppm)):7.78(d,2h,j=8.8hz),7.56-7.49(m,5h),7.40(s,1h),7.34-7.29(m,6h),7.13-6.98(m,8h),6.82(d,2h,j=8.8hz).hrms(maldi-tof)m/z526.1036(m+,calcd.526.1045).
化合物5和化合物11的合成
在一个装有冷凝管的100ml两颈圆底烧瓶中,将化合物3或者9(0.31mmol),4-羟基苯硼酸(0.045g,0.39mmol),碳酸钾(0.42g,3.06mmol)与pd(pph3)4(0.011g,0.0092mmol)在n2氛围下溶解在20ml蒸馏thf和3ml水中。混合物加热回流过夜。降到室温之后,混合物用二氯甲烷萃取3次。有机相水洗后用无水硫酸钠干燥。蒸干有机溶剂后得到粗产品。粗产品用硅胶色谱柱纯化,洗出液为二氯甲烷/乙酸乙酯(体积比99:1)。最终得到有机固体的产率为74%。
化合物5a:1hnmr(400mhz,cdcl3,·δ(ppm)):8.68(d,2h,j=4.4hz),8.68(d,2h,j=8.4hz),7.76-7.68(m,4h),7.55(d,2h,j=4.4hz),7.26(s,1h),6.74(d,2h,j=8.4hz),3.08(s,6h).13cnmr(100mhz,cdcl3,δ(ppm)):150.7,149.4,149.3,144.6,142.4,137.4,137.5,131.2,130.9,129.2,127.0,126.8,125.4,120.9,120.9,120.7,111.0,110.6,106.0,39.4,39.3.hrms(maldi-tof)m/z325.1575(m+,calcd.325.1579).
化合物5b:1hnmr(400mhz,cdcl3,·δ(ppm)):8.68(d,2h,j=4.4hz),7.82-7.76(m,1h),7.72(d,1h,j=8.0hz),7.66(d,2h,j=7.6hz),7.58(d,2h,j=8.0hz),7.52(d,2h,j=4.8hz),7.35-7.27(m,4h),7.18(d,2h,j=8.4hz),7.11-7.06(m,5h),6.83(d,2h,j=8.4hz).hrms(maldi-tof)m/z449.1916(m+,calcd.449.1892).
化合物5c:1hnmr(400mhz,cdcl3,·δ(ppm)):8.70(d,2h,j=5.6hz),8.00(d,2h,j=8.4hz),7.83(d,2h,j=8.4hz),7.74-7.68(m,4h),7.63(s,1h),7.55-7.52(m,4h),7.31-7.27(m,4h),7.16-7.14(m,6h),7.09-7.05(m,2h).hrms(maldi-tof)m/z525.2238(m+,calcd.525.2205).
化合物11:1hnmr(400mhz,cdcl3,·δ(ppm)):8.75(d,2h,j=4.0hz),7.99-7.95(m,4h),7.83(d,2h,j=8.4hz),7.76(d,2h,j=8.4hz),7.58(d,2h,j=5.6hz),7.54(d,2h,j=8.4hz),7.32-7.28(m,4h),7.17(d,2h,j=8.4hz),7.08(t,2h,j=7.2hz).hrms(maldi-tof)m/z550.4575(m+,calcd.550.2157).
化合物6和12的合成
在装有回流冷凝管的100ml两颈圆底烧瓶中,将5或11(0.154mmol)溶于5ml乙腈。加入0.1ml碘甲烷并且回流8h。冷却到室温后,将反应物逐滴加到乙醚中,会产生沉淀,过滤得到暗红色固体(产率95%)。将得到的固体溶于丙酮,加入5ml饱和kpf6溶液。将混合物搅拌1h,用压缩空气把溶剂吹干,有沉淀产生。过滤并且用水洗涤沉淀,得到黑色固体,产率95%。
化合物6a:1hnmr(400mhz,dmso-d6,δ(ppm)):8.98(d,2h,j=6.8hz),8.53(d,2h,j=6.8hz),8.18(d,2h,j=8.4hz),8.03(s,1h),7.93-7.40(m,4h),6.83(d,2h,j=8.8hz),4.29(s,3h),3.03(s,6h).13cnmr(100mhz,dmso-d6,δ(ppm)):153.0,152.0,145.3,144.4,138.3,132.0,131.6,128.5,125.6,123.5,120.3,118.9,111.4,100.3,46.8.hrms(maldi-tof)m/z340.1826(m+,calcd.340.1814).
化合物6b:1hnmr(400mhz,dmso-d6,δ(ppm)):8.95(d,2h,j=6.8hz),8.50(d,2h,j=6.8hz),8.17(d,2h,j=8.4hz),8.07(s,1h),7.95(d,2h,j=8.4hz),7.89(d,2h,j=8.8hz),7.39(t,4h,j=8.0hz),7.20-7.13(m,6h),6.93(d,2h,j=8.8hz),4.30(s,3h).hrms(maldi-tof)m/z464.2133(m+,calcd.464.2127).
化合物6c:1hnmr(400mhz,dmso-d6,δ(ppm)):8.97(d,2h,j=6.8hz),8.51(d,2h,j=6.8hz),8.23-8.19(m,3h),8.06-7.99(m,4h),7.85(d,2h,j=8.4hz),7.71(d,2h,j=8.4hz),7.33(t,4h,j=7.6hz),7.10-7.03(m,8h),4.30(s,3h).hrms(maldi-tof)m/z540.2458(m+,calcd.540.2440).
化合物12:1hnmr(400mhz,dmso-d6,δ(ppm)):9.01(d,2h,j=6.8hz),8.54(d,2h,j=6.8hz),8.28(d,2h,j=8.4hz),8.10(d,2h,j=8.4hz),7.96-7.89(m,4h),7.73(d,2h,j=8.8hz),7.35(t,4h,j=7.6hz),7.11-7.01(m,8h),4.33(s,3h).hrms(maldi-tof)m/z565.4226(m+,calcd.565.2392).
化合物9的合成
在n2条件下,在装有回流冷凝管的100ml两颈圆底烧瓶中,将7(0.62mmol)、8(0.045g,0.39mmol)、碳酸钾(0.42g,3.06mmol)和pd(pph3)4(0.011g,0.0092mmol)溶于20ml重蒸过的thf和3ml水。将反应液加热回流过夜。冷却到室温之后,用二氯甲烷萃取三次,收集有机相,用水洗涤,用无水硫化钠干燥。把溶剂旋蒸之后,粗产物用硅胶色谱柱纯化,洗脱液为二氯甲烷/乙酸乙酯(体积比为99:1)。得到橙色固体,产率为56%。
化合物9:1hnmr(400mhz,cdcl3,δ(ppm)):7.91(d,2h,j=8.8hz),7.74-7.69(m,5h),7.54(d,2h,j=8.8hz),7.34-7.28(m,5h),7.17(d,6h,j=8.4hz),7.08(d,2h,j=8.0hz).hrms(maldi-tof)m/z553.1021(m+,calcd.553.0977).
化合物16和17的合成
在n2条件下,将化合物13(0.5mmol)、14或15(0.5mmol)加到装有回流冷凝管的25ml两颈圆底烧瓶中。加入10ml干燥的乙醇,加热回流。加入2ml吗啉,反应2h。冷却到室温之后,用二氯甲烷萃取三次。收集有机相,用水洗涤,用无水硫化钠干燥。把溶剂旋蒸之后,粗产物用硅胶色谱柱纯化,洗脱液为正己烷/乙酸乙酯(体积比为7:3)。得到橙色固体,产率为56%。
化合物16:1hnmr(400mhz,cdcl3,δ(ppm)):7.46(d,2h,j=8.8hz),7.04(d,1h,j=16.0hz),6.92(d,2h,j=8.8hz),6.85(d,1h,j=6.4hz),6.80(s,1h),4.03(t,2h,j=6.4hz),3.72(t,4h,j=4.4hz),2.60(s,2h),2.46-2.39(m,8h),1.87-1.81(m,2h),1.72-1.65(m,2h),1.08(s,6h).hrms(maldi-tof)m/z432.2664(m+,calcd.432.2651).
化合物17:1hnmr(400mhz,cdcl3,δ(ppm)):7.42-7.40(m,2h),6.90(d,1h,j=16.0hz),6.70(s,1h),6.31(d,1h,j=6.4hz),6.09(d,1h,j=2.4hz),4.06(t,2h,j=6.4hz),3.72(t,4h,j=4.4hz),3.41(q,4h,j=7.2hz),2.56(s,2h),2.48-2.45(m,8h),1.96-1.89(m,2h),1.77-1.70(m,2h),1.21(t,6h,j=6.8hz),1.06(s,6h).hrms(maldi-tof)m/z502.3295(m+,calcd.502.3308).
化合物6(tpe-tetrad)的合成
丙二腈衍生物的合成参考了已报道过的文献。荧光分子tpe-tetrad(化合物6)的合成路线详见示意图。在n2条件下,将150mgpd(pph3)4、833mg(0.1.9mmol)2br-tpa-dcm、2.17g(5.8mmol)丙二腈衍生物2和1.5g(5mmol)k3po4加入反应瓶中,加入50mlthf和8ml水。将反应体系加热到70℃,反应36h。冷却到室温后,过滤,把滤液的溶剂旋干,粗产物用硅胶色谱柱纯化,洗脱液为正己烷/二氯甲烷。得到产物cho-tpa-2tpe900mg,产率为50%。
化合物7的合成
随后,边搅拌边将0.3ml哌啶加到198mg(0.2mmol)cho-tpa-2tpe和5ml乙腈的混合液中。加热到100℃反应72h。冷却到室温后,用100ml二氯甲烷萃取两次,水洗,无水硫酸钠干燥。过滤并将滤液的溶剂旋干,粗产物用硅胶色谱柱纯化,洗脱液为正己烷/二氯甲烷。得到产物红色粉末tpe-tetrad(化合物7)200mg,产率为40%。用1hnmr、13cnmr和高分辨质谱表征结构。
应当理解的是,对本领域普通技术人员来说,可根据上述说明加以改进或变换,所有这些改进或变换都应属于本发明所附权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!