一种检测6-单乙酰吗啡的试纸条及其制备方法和应用方法与流程
本发明涉及6-单乙酰吗啡的检测,具体是一种利用时间分辨荧光微球免疫层析技术定量检测6-单乙酰吗啡的试纸条及其制备方法和应用方法。
背景技术:
据联合国毒品和犯罪问题办公室发布的2018年《世界毒品报告》全面概述了阿片剂、可卡因、大麻、苯丙胺类兴奋剂和新型精神活性物质的供需情况及其对健康的影响。海洛因吸食和注射吸收良好,可大量穿透血脑屏障,迅速产生作用。服用海洛因后人体就会产生快感、幻觉感,导致依赖,甚至成瘾,给个人和社会造成极大的危害,对海洛因的检测已经引起社会的广泛关注。海洛因进入人体后在血脂酶的作用下迅速代谢成6-单乙酰吗啡,然后进一步在肝脏代谢成吗啡并与葡醛酸结合。体内吗啡可来源于滥用海洛因的代谢,也可来源于含吗啡或可待因的药物。而单乙酰吗啡仅来源于海洛因的代谢。因此,单乙酰吗啡的定性检出可作为确认滥用海洛因的证据。
目前检测6-单乙酰吗啡的常用方法有:酶联免疫吸附测定(elisa)、放射免疫测定(ria)、气相色谱-质谱联用法、液相色谱及液相色谱-质谱联用法等。这些色谱方法具有很好的灵敏度和特异性,但操作复杂,通量不高,耗时较长,仪器设备昂贵。酶联免疫吸附测定(elisa)以及胶体金免疫层析法是目前国际公认的主流技术,这两种方法具有检测速度快,价格便宜,操作简单等优点。但elisa检测仍需专业人员,且需要较长时间显示结果;胶体金法能对6-单乙酰吗啡进行定性分析,操作简单,检测时间较短,但灵敏度低、人为因素干扰较大。
综上所述,目前6-单乙酰吗啡的检测技术尚不成熟,开发一种灵敏度高、操作简便并且能够实现对大批量样品进行快速检测的产品和方法成为迫切需要解决的问题。
技术实现要素:
本发明的目的在于克服现有的检测6-单乙酰吗啡的方法存在的操作复杂、耗时较长,并且不能够实现对大批量样品的快速检测的特点,提供一种操作简单、灵敏度高、检测速度快、成本低的检测6-单乙酰吗啡的试纸条及其制备方法和应用方法,以实现对大批量的6-单乙酰吗啡样品进行快速检测和现场监控。
为了实现本发明的目的,本发明的一种检测6-单乙酰吗啡的试纸条采用以下技术方案:一种检测6-单乙酰吗啡的试纸条,包括样品吸收垫、结合物释放垫、反应膜、吸水垫和底板;其特征在于:所述的结合物释放垫上喷涂有时间分辨荧光微球标记的抗体;所述反应膜上包被有半抗原-载体蛋白偶联物的检测线和羊抗鼠二抗的质控线。
所述样品吸收垫、结合物释放垫、反应膜和吸水垫均粘贴在底板上且其中任意相邻两个沿上下方向部分叠加。
所述结合物释放垫的1/3-1/2被覆盖于样品吸收垫下。
所述时间分辨荧光微球是将直径为100nm-500nm的稀土离子作为标记物,时间分辨荧光微球的表面修饰有功能基团,用于蛋白、抗体和核酸的共价偶联。
所述时间分辨荧光微球的激发波长为300-400nm,发射波长为500-700nm。
所述样品吸收垫为玻璃纤维素膜。
所述结合物释放垫为玻璃纤维或聚酯材料。
所述反应膜为硝酸纤维素膜或醋酸纤维素膜。
所述底板为pvc底板或其他硬质不吸水的材料。
所述吸水垫为吸水纸。
本发明的一种制备上述检测6-单乙酰吗啡的试纸条的方法,包括以下步骤:
1)用荧光微球标记6-单乙酰吗啡抗体,并将其喷涂在结合物释放垫上,以制备喷涂有6-单乙酰吗啡单克隆抗体-荧光微球标记物的结合物释放垫;
2)将半抗原-载体蛋白偶联物和羊抗鼠二抗分别喷涂于反应膜上作为检测线(t)和质控线(c);
3)将1)和2)制备好的结合物释放垫、反应膜与样品吸收垫、吸水垫和底板组装成试纸条。
在步骤1)中取出荧光微球进行活化,然后加入6-单乙酰吗啡抗体进行共价偶联,结束后加入封闭缓冲液进行封闭,离心洗涤后放置于4℃保存备用。
在步骤1)中的结合物释放垫,先用缓冲液浸泡2h,37℃下烘干2h,置于干燥环境中保存,再用于喷涂标记的抗体。所述缓冲液是ph为7.4的0.02-0.05
mol/ltris-hcl缓冲液,其中含0.2-1%的牛血清白蛋白、0.1-5%的海藻糖和0.02-0.1%tween-20。
本发明的一种应用上述检测6-单乙酰吗啡的试纸条检测样品中6-单乙酰吗啡的方法,包括如下步骤:
(1)将试纸条和待测样品恢复至室温。
(2)开启免疫荧光分析仪,插入对应id卡,读取标准曲线。
(3)向试纸条的样品孔中加入待测样本60-120μl,反应5-10min后,将检测卡插入免疫荧光分析仪。
(4)截留在检测线和质控线的荧光微球在最佳激发光下,发出强烈的荧光条带;
(5)采用免疫层析分析仪读取检测线和质控线的荧光强度,并给出t/c值,分析仪可通过内置的标准曲线计算出样品中6-单乙酰吗啡的浓度,并判断阴阳性。
本发明与现有技术相比,有如下优点:
(1)本发明能够准确定量待测样本中的6-单乙酰吗啡的含量。
(2)本发明采用独立的质控线和检测线的反应系统,互不干扰和影响,并采用t/c值的方式进行标定,保证了测试结果的准确性。
(3)本发明采用时间分辨荧光微球,由于其stokes位移大(>150nm)且荧光寿命比本底物质荧光寿命高5~6个数量级,能够有效地消除各种非特异性荧光的干扰,提高检测的灵敏度。
(4)本发明提供了对于毛发、血液、唾液、尿液等生物样本的快速前处理方法,保证了测试的快速。
本发明的试纸条具有灵敏度高、特异性强、成本低、操作简单、检测时间短、不受检测设备限制、储存简单、保质期长的优点。用本发明试纸条检测6-单乙酰吗啡的方法,简便、快速、准确、适用范围广、成本低、易推广使用。
进一步地,结合物释放垫的1/3-1/2被样品吸收垫覆盖可以延长检测结果观察时间,可使样品吸收垫将检测液体充分吸收并与抗体充分反应,从而减少误差。
附图说明
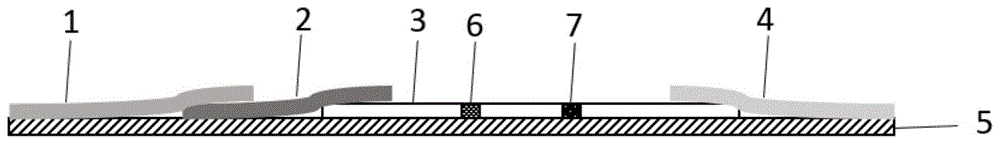
图1是是本发明的一种检测6-单乙酰吗啡的试纸条的结构示意图。其中1是样品吸收垫,2是结合物释放垫,3是反应膜,4是吸水垫,5是底板,6是检测线,7是质控线。
图2是检测卡的结构示意图。其中8是检测窗,9是样品孔
图3是试纸条样品检测结果示意图。
图4是本发明试纸条的标准曲线。
图5是唾液采集装置结构示意图。其中10是采集槽盖,11是采集槽,12是采集管,13是采集管盖,14是最低收集线。
具体实施方式
下面结合具体的实施例来进一步阐述本发明。应理解,这些实施例仅用于说明本发明,而不用来限制本发明的范围。另外,本领域的技术人员在所附权利要求书限定的范围内可能会对本发明进行各种改动或修饰,这些改动或修饰同样应落入发明的保护范围。
本发明的一种检测6-单乙酰吗啡的试纸条,如图1所示,包括样品吸收垫、结合物释放垫、反应膜、吸水垫和底板;结合物释放垫上喷涂有时间分辨荧光微球标记的抗体;反应膜上包被有半抗原-载体蛋白偶联物的检测线t和羊抗鼠二抗的质控线c。样品吸收垫、结合物释放垫、反应膜和吸水垫均粘贴在底板上且中任意相邻两个沿上下方向部分叠加。结合物释放垫的1/3被样品吸收垫覆盖可以延长检测结果观察时间,可使样品吸收垫将检测液体充分吸收并与抗体充分反应,从而减少误差,在其他实施例中,也可以结合物释放垫的1/2被覆盖于样品吸收垫下。时间分辨荧光微球是直径为100nm-500nm的稀土离子作为标记物的荧光微球,其表面修饰有功能基团,用于蛋白、抗体和核酸的共价偶联。时间分辨荧光微球的激发波长为300-400nm,发射波长为500-700nm。样品吸收垫为玻璃纤维素膜。结合物释放垫为玻璃纤维或聚酯材料。反应膜为硝酸纤维素膜或醋酸纤维素膜。底板为pvc底板或其他硬质不吸水的材料。吸水垫为吸水纸。
该检测6-单乙酰吗啡的试纸条的制备方法主要包括以下步骤:
1)用荧光微球标记6-单乙酰吗啡抗体,并将其喷涂在结合物释放垫上,以制备喷涂有荧光微球标记的6-单乙酰吗啡抗体的结合物释放垫;
2)将半抗原-载体蛋白偶联物和羊抗鼠二抗分别喷涂于反应膜上作为检测线(t)和质控线(c),以制备包被有6-单乙酰吗啡半抗原-载体蛋白偶联物的检测线和包被有羊抗鼠二抗的质控线的反应膜;
3)将1)和2)制备好的结合物释放垫、反应膜与样品吸收垫、吸水垫和底板组装成试纸条。
下面分步详细叙述:
1、荧光微球标记物的制备:
荧光微球标记6-单乙酰吗啡抗体的制备:取1mg荧光微球15000rpm离心10min,收集沉淀,用1ml偶联缓冲液重悬沉淀。然后按1:2-1:20的摩尔比加入edc和nhs,涡旋震荡后室温孵育20-30min,15000rpm离心10min,收集沉淀。加入偶联缓冲液重悬微球,向该溶液中加入40-150μg6-单乙酰吗啡抗体,充分混匀后,室温搅拌反应2-4h,10000rpm离心10min去上清,加入1ml封闭缓冲液,混匀后室温反应1-2h,用封闭缓冲液离心洗涤3次后,用0.02mph7.4的pbs(含0.2-1%bsa和0.1-5%海藻糖)重悬沉淀,即为制备好的荧光微球标记的6-单乙酰吗啡的抗体,放置于4℃备用。
2、荧光微球垫的制备:
将结合物释放垫垫用含0.2-1%牛血清白蛋白(质量分数)、ph7.4的0.02-0.05mtris-hcl(含0.1-5%的海藻糖和0.02-1%tween-20)缓冲液浸泡2h,37℃下烘干2h备用。用喷膜仪将荧光微球标记的6-单乙酰吗啡的抗体喷涂至结合物释放垫上,每1cm结合物释放垫喷涂1-9μl荧光微球标记的6-单乙酰吗啡抗体,37℃干燥1-2h,置于干燥环境中备用。
3、nc膜的制备:
将6-单乙酰吗啡半抗原-载体蛋白偶联物和羊抗鼠抗体分别包被于nc膜上:用0.02mph7.4的pbs将6-单乙酰吗啡半抗原-载体蛋白偶联物调节至0.5-2mg/ml,包被在nc膜上形成检测线,包被量为5-10μl/cm;用0.01mph7.4的pbs将羊抗鼠二抗调节至0.1-0.5mg/ml,包被在nc膜上形成质控线,包被量为5-10μl/cm。将包被好的反应膜置于37℃干燥1-2h,置于干燥环境中备用。
4、时间分辨荧光微球免疫检测卡的制备
在pvc底板上依次粘贴样品吸收垫,喷涂有荧光微球标记的6-单乙酰吗啡抗体的结合物释放垫,喷涂有6-单乙酰吗啡半抗原-载体蛋白偶联物作为检测线和羊抗鼠二抗作为质控线的反应膜,吸水垫;其中,结合物释放垫从起始端有1/3区域被样品吸收垫覆盖,结合物释放垫的末端与反应膜的始端连接,反应膜的末端与吸水垫的始端相连,样品吸收垫的始端与pvc底板的始端对齐,吸水垫的末端与pvc底板的末端对齐;所述反应膜上的检测线和质控线与所述试纸条的长相呈垂直的条状带;检测线位于靠近结合物释放垫的末端的一侧;质控线位于远离结合物释放垫的末端的一侧;组装完成后剪切成4mm的宽度,即成为免疫层析试纸条。
把免疫层析试纸条固定在塑料底卡上,试纸条表面用面卡压紧,面卡在对应试纸条样品吸收垫和nc膜的部分分别预留样品孔9和检测窗8,如图2所示。该检测卡组装好后装入铝箔袋,加入干燥剂封口,放置于室温干燥环境下可保存12个月。
一种应用上述试纸条检测样品中6-单乙酰吗啡的方法,该方法包括以下步骤:
1)将试纸条和待测样品恢复至室温;
2)开启免疫荧光分析仪,插入对应id卡,读取标准曲线;
3)向试纸条的样品孔9中加入待测样本60-120μl,反应5-10min后,将检测卡插入免疫荧光分析仪;
4)截留在检测线和质控线的荧光微球在最佳激发光下,发出强烈的荧光条带;
5)采用免疫层析分析仪读取检测线和质控线的荧光强度,并给出t/c值,分析仪可通过内置的标准曲线计算出样品中6-单乙酰吗啡的浓度,并判断阴阳性,如图3所示。
试验例1毛发样品中6-单乙酰吗啡含量的检测
1、6-单乙酰吗啡检测试纸条标准曲线的建立
取空白毛发样品,剪碎后涡旋或超声或研磨,在处理后的溶液中分别添加6-单乙酰吗啡至终浓度为0.1ppb、0.25ppb、0.5ppb、1ppb、2ppb、4ppb、8ppb、16ppb,取试纸条进行检测,每个样品重复测定五次。将测定的五次重复结果取平均值后,在免疫荧光分析仪上进行标定。
2、毛发样品中6-单乙酰吗啡的检测
(1)样本的前处理
①检测前将样本恢复至室温20-25℃;
②称取20-50mg毛发样本剪碎至聚苯乙烯离心管中;
③加入1ml样品提取液,水浴超声3min;
(2)用试纸条进行检测
①开启免疫荧光分析仪,插入对应id卡,读取标准曲线。
②正面朝上平放检测卡,向试纸条的样品孔中加入待测样本60-120μl,室温反应5-10min后,将检测卡放入免疫荧光分析仪中进行检测
③截留在检测线和质控线的荧光微球在最佳激发光下,发出强烈的荧光条带;
④采用免疫层析分析仪读取检测线和质控线的荧光强度,并给出t/c值,分析仪可通过内置的标准曲线计算出样品中6-单乙酰吗啡的浓度,并判断阴阳性。
试验例2血液样品中6-单乙酰吗啡含量的检测
该实施例中,试纸条所有制备方法与实施例1相同,除样品吸收垫为滤血膜。
1、溶血血液样品
(1)6-单乙酰吗啡检测试纸条标准曲线的建立
取空白血液样品,用样品稀释液按1:5-1:20的比例进行稀释,向稀释后的溶血血液样品溶液中分别添加6-单乙酰吗啡至终浓度为0.1ppb、0.25ppb、0.5ppb、1ppb、2ppb、4ppb、8ppb、16ppb,取试纸条进行检测,每个样品重复测定五次。将测定的五次重复结果取平均值后,在免疫荧光分析仪上进行标定。
(2)溶血血液样品中6-单乙酰吗啡的检测
①样本的前处理
a检测前将样本恢复至室温20-25℃;
b用样品稀释液按1:5-1:20的比例对溶血血液样品进行稀释。
②用试纸条进行检测
a开启免疫荧光分析仪,插入对应id卡,读取标准曲线。
b正面朝上平放检测卡,向试纸条的样品孔中加入待测样本60-120μl,室温反应5-10min后,将检测卡放入免疫荧光分析仪中进行检测
c截留在检测线和质控线的荧光微球在最佳激发光下,发出强烈的荧光条带;
d采用免疫层析分析仪读取检测线和质控线的荧光强度,并给出t/c值,分析仪可通过内置的标准曲线计算出样品中6-单乙酰吗啡的浓度,并判断阴阳性。
2、新鲜血液样品
该实施例与上述溶血血液样品实施例相同,但是新鲜血液样品测试前无需稀释可直接加样进行检测。
试验例3尿液样品中6-单乙酰吗啡含量的检测
该实施例中,试纸条所有制备方法与样品检测方法与实施例1-2相同。
试验例4唾液样品中6-单乙酰吗啡含量的检测
该实施例中,试纸条所有制备方法与样品检测方法与实施例1-2相同,唾液的采集会用到唾液采集装置,如图5所示,包括采集槽盖10,采集槽11,采集管12,采集管盖13,采集管12上设置有最低收集线14。
唾液样品的采集按照如下步骤进行:
1、将唾液吐进采集槽中直至唾液量达到最低采集线。
2、将采集槽盖盖紧,直到听见咔嗒声,盖子中的样品稀释液流入采集管中,与唾液样品混和。
3、将采集槽拧下,盖上采集管盖,上下颠倒混匀。
4、吸取稀释后的唾液样品进行检测。
基本参数的建立
检出限:用空白样品进行重复测定20次,计算20次结果的均值m与标准差sd,以空白均值加两倍标准差(m+2sd)报告方法的检测限,结果为0.05ppb。线性范围:取0.1ppb、0.25ppb、0.5ppb、1ppb、2ppb、4ppb、8ppb、16ppb,,等浓度值进行检测,每个浓度重复测量五次,将测定浓度平均值与理论值进行线性分析,得到线性方程y=-2.7414x-0.9307,,r2=0.9804。(实验结果及分析见表1、图4)。
表16-单乙酰吗啡标准品检测结果
准确度:用样品稀释液配制浓度为5ppb的6-单乙酰吗啡标品,用实施例1中所制备试纸条进行检测,重复检测三次,检测结果取平均值进行计算。回收率=检测浓度/实际加入浓度×100%,计算得样品回收率为103.5%。
精密度:取三批实施例1中所制备的时间分辨荧光定量6-单乙酰吗啡检测试纸条,检测5ppb浓度标品,每批试纸条标品平行检测10次,结果显示,三批批次内cv值分别为7.334%,8.904%,7.497%,三批批次间cv值为8.859%。
从上述数据可以看出,本发明所述试纸条,相比现有的检测6-单乙酰吗啡的方法,具有更灵敏、更快速、可准确定量的特点,不受操作地点的限制,且配套的检测仪器小巧轻便,人员要求更低,适合大范围的推广使用。
- 还没有人留言评论。精彩留言会获得点赞!