一种采用调幅电场治疗肿瘤的装置的制作方法
本发明属于医疗器械的技术领域,涉及一种采用调幅电场治疗肿瘤的装置。
背景技术:
自1980年起,电场就被普遍用于生物和医学领域,涵盖杀死微生物、细胞融合、基因转化和肿瘤治疗等。2004年Yoram Pati等发现低电场强度1V/cm~2V/cm、中低频(100~300KHZ)的AC电场能选择性地抑制肿瘤细胞增殖。随着肿瘤治疗电场(Tumor Treating Fields,TTF)作用机制等的研究,TTF作为一种新的肿瘤治疗方法,相较于传统的手术、放化疗有许多潜在性优势。吴清辉等报道:第一,TTF将绝缘电极置于恶性肿瘤病灶部位外周的皮肤,可覆盖能发生癌变的几乎所有部位;第二,TTF治疗的副作用除了绝缘电极片与皮肤接触部位可能发生轻度皮炎外,尚未见报道出现其它不良反应,也不会对心脏、神经组织产生影响;第三,TTF与化疗药物合用时不会加重化疗药物的毒性反应;第四,TTF作为可佩戴的设备,患者可随意安排时间自行治疗,却不影响日常生活。
TTF具有彻底改变实体瘤治疗规范的潜力。文献报导,在各种体外和活体实验中,TTF显示出可抑制多种癌细胞增殖、诱导癌细胞凋亡的能力,如对人黑色素瘤细胞、前列腺癌细胞、乳腺癌细胞等均有疗效,对进展期非小细胞肺癌(NSCLC)也有一定的抑制能力。Salzberg等的研究还发现TTF对乳腺原发的转移瘤和间皮细胞瘤可能存在抑制作用。TTF对转运蛋白的多药耐药的卵巢癌和乳腺癌细胞系也有抑制作用。此外还有研究指出,TTF不仅可用于治疗原发部位的进展期肿瘤,还可防治转移性肿瘤。TTF可以阻止转移瘤再转移,特别是阻止肺转移瘤的生长与进展,Kirson等采用TTF治疗植入黑色素瘤细胞(B16F 10)的小鼠与VX-2型鳞癌细胞的新西兰兔,发现治疗组肿瘤肺转移率明显低于对照组,且动物生存期长,符合可抑制恶性实体瘤细胞转移、播散和增长的理论。
TTF可联合化疗运用于肿瘤的维持治疗和放疗难以实施的紧急治疗。在与化疗联用的研究方面,Miklos等的临床试验证实,TTF结合培美曲塞可安全有效地治疗进展性肺小细胞肺癌(SCLC)。同时,TTF与培美曲塞结合治疗晚期非小细胞肺癌的I/II临床试验也证明了TTF治疗的高效性与安全性,患者的中位生存期在较常见的8.3个月基础上延长了5.5个月,治疗的总有效率也从9.1%上升到14.6%,因此TTF联合培美曲塞治疗方案优于单药。Kirson等在应用紫杉醇+阿霉素+环磷酰胺+达卡巴嗪联合TTF处理乳腺癌细胞系(MDA-MB-231)和人胶质瘤细胞系(U-118)时发现,结合TTF治疗后上述肿瘤细胞对化疗的敏感性上升了1~3个数量级,化疗功效与敏感性均得到提高。Morant等还开展了对TTF结合4疗程新辅助化疗(表柔比星+多西他赛)治疗恶性乳腺癌的研究,以评估TTF对乳腺癌术前化疗的影响。
综合文献报导,TTF的作用机制主要是干扰破坏细胞的有丝分裂。有丝分裂是人体细胞的主要分裂方式。细胞由间期进入分裂期后开始分裂。首先细胞内的中心粒互相分开,并向细胞两端移动,中间以细丝(纺锤丝)相连;在中心粒分开的同时细胞核膨大、染色质浓缩、核仁核膜消失,染色体已复制纵裂为二,其着丝点与两端的纺锤丝相连并移向细胞两端,最后又恢复成染色质状态,核仁与核膜重新出现,各自形成一个新的细胞核;在细胞核形成的同时,细胞质也分成两等分,细胞膜从中部凹陷(即形成有丝分裂沟)隔开,这样形成两个新细胞而完成有丝分裂。如果在细胞有丝分裂过程中施加不均匀的外电场,则在有丝分裂前期使由有极分子组成的微管发生转向极化并沿着场强较强的方向移动,致使微管不能集聚成纺锤丝,造成细胞有丝分裂中止;同时施加的外部电场力线方向与分裂细胞长轴平行时,可造成有丝分裂末期细胞狭小的有丝分裂沟处的电场力线与细胞质的密度最高,在库仑力的作用下,有丝分裂沟处的细胞膜发生破裂而不能分裂出两个完整的新细胞。
目前全球只有诺沃库勒(Novocure)有限公司开发的NOVOTTF-100A中频交变电场肿瘤治疗设备用于临床,所述设备于2011年通过美国FDA的审批,作为复发性变形性脑胶质母细胞瘤一线治疗失败后的二线治疗。诺沃库勒有限公司在中国申请的专利(CN1976738B,发明名称为使用不同频率的电场治疗肿瘤),其专利权利要求的装置包括AC电压源、绝缘电极;当绝缘电极低靠病人放置时,在靶区域中按时间顺序地施加具有第一频率的第一AC电场和具有第二频率的第二AC电场以提供重复的频率循环,第一和第二电场的频率的专利权利要求的组合分别为:50KHZ到500KHZ、100KHZ至300KHZ、170KHZ至250KHZ、100KHZ至300KHZ,其专利权利要求的电场频率属于中低频率,并以低频为主(按频率划分标准低频一般为30~300KHZ,中频一般为300~3000KHZ)。
目前现有的电场治疗设备及技术是采用固定场强的多个频率的电场治疗,有其缺陷性。第一,文献报导不同种类的肿瘤对场强的敏感性不同,例如体外试验中恶性黑色素瘤细胞对1.4V/cm的电场强度最为敏感,而2.5V/cm的电场强度对神经胶质瘤的抑制最强。固定强度的电场用于治疗肿瘤时,电场力线从皮肤到达肿瘤病灶区前需要穿过正常区域,正常区的细胞、组织、器官存在不同大小的阻抗作用可引起电场力线的畸变,故难以确定肿瘤细胞所遭受的真实电场强度,无法施加强度精准的电场,有可能施加的电场强度达不到治疗的效果或效果不理想。第二,作用机制单一,如前所述TTF的作用机制体现为两方面的作用,一方面是施加不均匀的外部电场,在细胞有丝分裂的前期干扰纺锤丝的形成而中止细胞的有丝分裂;另一方面在细胞分裂的末期,在细胞中部形成狭小的有丝分裂沟,当外部电场力线与分裂细胞长轴平行时有丝分裂沟处的电场力线与细胞质的密度最大,在库仑力作用下狭小的有丝分裂沟处的细胞膜容易发生破裂。现有技术采用强度固定而频率变化的电场刺激,由于施加的是均匀的外电场,不具有在细胞有丝分裂的前期干扰纺锤丝的形成而中止细胞有丝分裂的作用机制。第三,其选择的电场频率以低频为主,可产生低频电流,低频电流施加到人体导致具有潜在危害的细胞内离子浓度变化(如细胞内Ca2+浓度增加,细胞外Ca2+浓度下降),并在组织的介质中发生电解形成有害物质,一旦绝缘电极绝缘层失效或击穿后则低频电流可造成机体的严重损害,故其临床应用存在安全隐患。
诺沃库勒有限公司的专利(CN 1976738B)未涉及电场强度连续变化与肿瘤治疗相关联的内容,其发明装置未注明调幅单元;其电场强度要求的范围当采用低频时为1V/cm~5V/cm,当采用中低频时为0.1V/cm~10V/cm,可理解为其使用的电场强度为此范围内的某固定强度,而不是在此范围内连续变化的电场强度。专利要求是通过使用具有两个或更多频率(50KHZ至约500KHZ)的电场实现改进的效果,其陈述的电场治疗机制是通过对细胞膜的“锤击”效应造成有丝分裂沟处细胞膜的破裂,未涉及到不均匀的外电场干扰阻碍纺锤丝形成的电场作用机制,这也佐证了其电场为强度不变化的均匀电场。
到目前为止,国内对TTF治疗肿瘤研究方面的报道极为少见,主要是因为缺乏相应的仪器设备。国内的肿瘤研究与临床治疗机构迫切需要一种多功能电场设备,用于开展有关TTF治疗肿瘤方面的研究。第一,需要研究电场各刺激因素与时间等参数与疗效的量效关系,尤其需要体外研究对各型肿瘤细胞实施外电场刺激能产生杀灭或抑制效果最大的刺激强度即敏感强度,这些外电场刺激包括电场强度、电场频率、电流等。第二,TTF具有彻底改变实体瘤治疗规范的潜力,但更多的基础研究和临床试验也亟待深入。例如,在治疗方式上,TTF可联合化疗运用于肿瘤的维持治疗或手术和放疗难以实施的紧急治疗,TTF结合化疗的优势机制尚待研究。TTF对不同类型肿瘤细胞敏感的刺激因素尚不明确,与放化疗等治疗手段相结合的优劣也鲜有报道,在治疗实体肿瘤方面的作用及权重大小也有待探讨,如何使治疗优势最大化也需进一步探索。因此需要一种多功能的电场设备用于包括基础研究、临床预试验、临床治疗等多方面的研究,使电场对肿瘤的治疗优势在国内得到充分发挥。
现有的集成中频电流电场治疗肿瘤的技术,对于表层肿瘤是可行的,但不适用于深部肿瘤的治疗。因为上皮细胞具有极性,上皮组织覆盖于身体表面及体内各种管道、囊腔的内面,上皮组织细胞比其它组织细胞导电性能好,当在机体表面施加电流时,电流主要从体表传导,很难将其准确传导到深部肿瘤病灶上,其靶向性较差,对正常组织细胞的损害大。同时未调制的中频电流的幅度无变化,易为肿瘤细胞所适应使治疗的效果有限。为了克服中频电流的这一弱点,可采用低频调制的中频电流,使中频的幅度产生低频的变化,电流的频率、波型、幅度可不断变化,肿瘤细胞不易产生适应性,人体组织的阻抗明显下降不发生电解作用,没有低频电流的作用表浅、对皮肤刺激大、有电解作用等缺点。
技术实现要素:
本发明的目的是提供一种采用调幅电场治疗肿瘤的装置,一是用以解决现有技术的电场作用机制单一治疗效果有限,电场强度固定不变不能确保肿瘤细胞遭受其敏感强度的电场刺激,电场频率以低频为主的低频电流一旦施加到人体造成意外伤害等问题。二是通过在一对绝缘电极间产生电场强度连续交替变化的调幅电场,作为不均匀的外电场用于肿瘤治疗;三是用于国内开展与TTF相关的研究工作。
为实现上述目的,本发明提供的技术方案是:一种采用调幅电场治疗肿瘤的装置,该装置包括:中央控制单元,用于各个单元协调控制;调频信号发生单元,用于产生各种频率信号;幅度调制单元,用于调制产生幅度连续交替变化的调幅波信号,调制波为正弦波形则产生幅度平缓而连续交替变化的调幅波信号,或者调制波为锯齿波形则产生幅度剧烈而连续交替变化的调幅波信号;功率放大单元,用于放大幅度调制单元产生的调幅波信号;输出分配单元,用于放置的调幅信号的分配与输出;绝缘电极,用于形成连续交替变化的调幅电场;绝缘电极定位系统,根据由电脑模态图提供的病灶的体积、位置、深度、病灶区域机体外形特征等信息,确定绝缘电极的最佳分布位置。
本发明的采用调幅电场治疗肿瘤的装置,其调频信号发生单元采用直接数字频率合成器或由变容二极管组成的调频电路,其幅度调制单元采用正弦波晶体管调幅电路、锯齿波晶体管调幅电路、正弦波集成电路调幅电路或锯齿波集成电路调幅电路,其功率放大单元采用中频功率放大电路,输出分配单元采用分配控制电路和电子开关来实施。
本发明的采用调幅电场治疗肿瘤的装置,其一对绝缘电极间产生强度连续交替变化的调幅电场,这种调幅电场作为不均匀的外电场,施加到分裂期的肿瘤细胞上,一方面干扰破坏肿瘤细胞的有丝分裂,另一方面确保使肿瘤细胞遭受到其敏感强度的电场刺激,从而对肿瘤实施电场强度相对精准的治疗。
本发明的采用调幅电场治疗肿瘤的装置,其n对绝缘电极安装在绝缘电极固定支架上并通过中央控制单元控制,相邻两对绝缘电极同时工作一次,或每对绝缘电极交替轮换工作一次,产生2n个调幅电场同时交叉重叠覆盖在病灶上。
本发明的采用调幅电场治疗肿瘤的装置,其绝缘电极由导电材料制造,外表为绝缘层,绝缘电极的朝外一面设置扣式导线连接点,绝缘电极上下分别有上固定桩和下固定桩,上固定桩和下固定桩均采用绝缘材料;上固定桩为套管弹簧顶压结构,套管弹簧顶压结构包括套管及凸字形桩头和弹簧,凸字形桩头和弹簧被封装在上端开口口径小于内径的套管内,凸字形桩头的小头被弹簧以较大压力顶出套管上端开口;绝缘电极安装到绝缘电极底座上,上固定桩卡入绝缘电极底座的上安装糟,下固定桩卡入绝缘电极底座的下安装糟,弹簧使上固定桩和下固定桩分别紧紧顶住绝缘电极底座内的上安装糟和下安装糟,绝缘电极可绕上固定桩和下固定桩形成的轴转动以适应人体不同部位的外形。
本发明的采用调幅电场治疗肿瘤的装置,绝缘电极定位系统采用适形模态计划系统;适形模态计划系统根据患者影像信息,提供的病灶体积、位置、深度,结合病灶区机体外形特征,由电脑合成模态图;通过电脑模态图优选出一对或多对绝缘电极在病灶部位的最佳绝缘电极分布图,以实现绝缘电极位置相对精准的电场治疗。
本发明的采用调幅电场治疗肿瘤的装置,其绝缘电极固定支架为由多节单元结构组成的链条式支架,用于抵靠固定在人体上,绝缘电极固定支架采用不导电材料,绝缘电极固定支架的每一节单元结构有一个绝缘电极底座;绝缘电极固定支架裸用,或者绝缘电极固定支架置于头盔或衣服内使用。
本发明的采用调幅电场治疗肿瘤的装置,中央控制单元采用微型触屏工业平板电脑、或单片机、或PC电脑或者手机终端;中央控制单元还包括人机交互单元;装置还包括电源。
本发明的采用调幅电场治疗肿瘤的装置,在中央控制单元控制下,调频信号发生单元产生的频率信号,传导到幅度调制单元后不采用低频调制传导到功率放大单元,或者调频信号发生单元产生的频率信号直接传导到功率放大单元,通过控制功率放大单元的放大倍数连续交替变化使频率信号产生所需要的幅度变化。
本发明的一种采用调幅电场治疗肿瘤的装置,在实施电场对肿瘤的治疗模式时,作用机制是将一对绝缘电极间产生强度连续交替变化的调幅电场作为不均匀的外电场施加到肿瘤细胞上,干扰破坏肿瘤细胞的有丝分裂。分裂前期细胞遭受不均匀的外电场作用时,一方面细胞内微管发生转向极化,使微管由原取向的杂乱无章转至与外部电场一致的方向排列,同时受到合外力的作用,使微管向场强较强的方向移动,这样造成微管不能集聚成纺锤丝而中止细胞的有丝分裂;另一方面分裂细胞内的微管等由有极分子组成的细胞质发生转向极化后向着场强较强的方向移动,当外部电场力线方向与细胞分裂长轴平行时,有丝分裂末期细胞的有丝分裂沟处的电场力线密度最高,使两个亚细胞内的由有极分子组成的细胞质移动并汇集在狭小的有丝分裂沟处,在库仑力作用下,由有极分子组成的细胞质发生随电场强度与频率不同的振动,使有丝分裂沟处的细胞膜遭受更大并具有“锤击”效应的力而发生破裂。另外,根据体外试验得出的各肿瘤细胞敏感的电场强度,施加强度在以肿瘤细胞敏感电场强度为中间值的一定范围内的连续交替变化的电场时,确保使肿瘤细胞遭受其敏感强度的电场刺激。
本发明的技术效果:
本发明的一种采用调幅电场治疗肿瘤的装置,通过一对绝缘电极间产生强度连续交替变化的调幅电场,作为不均匀的外电场施加到肿瘤细胞上,既在细胞有丝分裂前期造成肿瘤细胞内的微管不能集聚成纺锤丝而中止细胞的有丝分裂,又在细胞有丝分裂末期通过合外力等因素的共同作用下,造成肿瘤细胞有丝分裂沟处的细胞膜发生破裂,故对肿瘤的治疗是双重机制。同时使用电池作电源,在没有交流电源的环境下采用锂电池作电源使用2~4小时,在电池备份的情况下连续使用4~8小时,方便携带式使用。现有的电场治疗设备及技术是通过具有两个或更多频率(50KHZ至约500KHZ)的电场实现改进的效果,其治疗机制仅是造成肿瘤细胞有丝分裂沟处的细胞膜发生破裂而用于肿瘤治疗,其治疗机制单一;并要求设备采用AC电源,不方便携带式使用。
本发明的一种采用调幅电场治疗肿瘤的装置,根据体外试验得出的各类肿瘤细胞敏感的电场强度,向肿瘤细胞施加强度在以肿瘤细胞敏感电场强度为中间值的一定范围内的连续交替变化的调幅电场时,确保使肿瘤细胞遭受其敏感强度的电场刺激。而现有的电场治疗设备与技术因电场强度固定不能在一定范围内连续交替变化,无法确保使肿瘤细胞遭受其敏感强度的电场刺激,有可能施加的电场强度达不到治疗效果或效果不理想。
本发明的一种采用调幅电场治疗肿瘤的装置,是在一对绝缘电极间产生强度连续交替变化的调幅电场,其治疗的双重作用机制对调幅电场覆盖区域的所有分裂的细胞均有作用。现有的电场治疗装置与技术是采用不同频率的电场刺激,其造成有丝分裂沟处细胞膜破裂的单一作用机制,仅对分裂细胞长轴与外部电场力线方向平行的分裂细胞有效。
本发明的一种采用调幅电场治疗肿瘤的装置,采用两对以上不同形状与大小的绝缘电极,安装在多节组成的链条式绝缘电极支架上,经过调整与固定可形成多个外电场交叉重叠覆盖肿瘤病灶区域。当外电场力线与分裂细胞长轴平行时,有丝分裂沟处的细胞膜容易发生破裂,而实际情况是肿瘤细胞分布是无序的,各肿瘤分裂细胞长轴方向是杂乱无章的。当n对绝缘电极按单对绝缘电极轮换工作一次和相邻两对绝缘电极轮换同时工作一次,则电场方向改变了2n次,一方面使外电场力线与肿瘤分裂细胞长轴平行的概率显著增加,使更多的肿瘤细胞发生有丝分裂沟处的细胞膜破裂;同时肿瘤病灶区的累计电场刺激为单对绝缘电极工作一次的2n倍,则肿瘤病灶邻近区域的正常组织细胞累计遭受的电场刺激相当于肿瘤病灶区域的2n分之一。而现有的电场治疗设备通过不同频率的第一AC电场与第二AC电场提供重复的频率循环,施加的电场个数少,单对电极使用的重复次数多,肿瘤分裂细胞长轴与外电场力线方向平行的概率低,肿瘤细胞发生有丝分裂沟处的细胞膜破裂的数量少,肿瘤病灶邻近区域的正常组织细胞遭受的电场刺激相当于肿瘤病灶区域的二分之一。
本发明的一种采用调幅电场治疗肿瘤的装置,在调幅单元将中频载波采用低频(或超低频)调制波调制时,调制的中频电流克服了中频电流的幅度无变化不易为人体感知的缺点,同时当绝缘电极绝缘层失效或绝缘电极被击穿时,防止低频电流施加到人体导致潜在危害的发生(例如细胞内离子浓度变化和在组织的介质中发生电解形成有害物质),提高临床使用的安全性。
本发明的一种采用调幅电场治疗肿瘤的装置,其绝缘电极定位系统采用适形模态计划系统;适形模态计划系统根据患者影像信息提供的病灶体积、位置、深度,结合病灶区机体外形特征,由电脑合成模态图;通过电脑模态图优选出一对或多对绝缘电极在病灶部位的最佳绝缘电极分布图,以实现绝缘电极位置相对精准的电场治疗。
附图说明
图1A在均匀的外电场下偶极子所受的力矩示意图;
图1B在均匀的外电场下偶极子转向示意图;
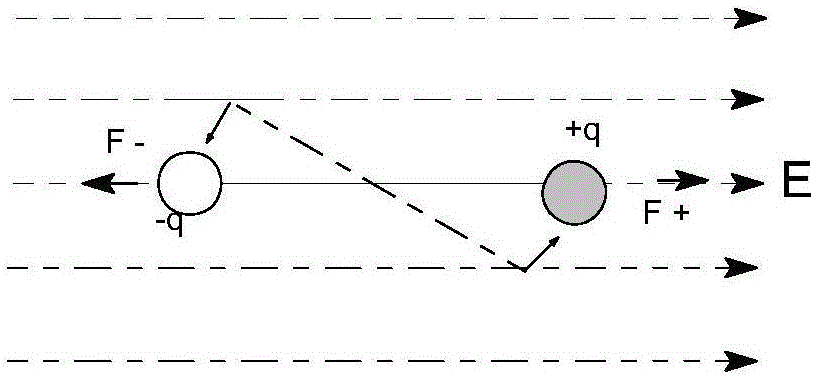
图2A在非均匀的外电场下偶极子所受的力矩示意图;
图2B在非均匀的外电场下偶极子所受的转向示意图;
图3细胞有丝分裂模式图;
图4正弦波调制的调幅波的形态示意图;
图5有丝分裂末期细胞中的外部电场力线传导示意图;
图6装置的架构示意图;
图7A幅度调制单元的电路工作示意图;
图7B锯齿波形调制波示意图
图7C正弦波波形的载波示意图
图7D锯齿波调制的调幅波形态示意图
图8功率放大单元示意图;
图9输出分配单元示意图;
图10链条式绝缘电极固定支架未安装绝缘电极的整体示意图;
图11链条式绝缘电极固定支架安装不同形状与大小的绝缘电极的整体示意图;
图12绝缘电极底座结构示意图;
图13绝缘电极结构示意图;
图14绝缘电极安装于绝缘电极底座的示意图;
图15多对绝缘电极交叉重叠病灶时绝缘电极对应位置示意图。
具体实施方式
图1A在均匀的外电场下偶极子所受的力矩示意图;图1B在均匀的外电场下偶极子转向示意图;图2A在非均匀的外电场下偶极子所受的力矩示意图;图2B在非均匀的外电场下偶极子所受的转向示意图;图3细胞有丝分裂模式图;图4正弦波的调幅波的形态示意图;图5有丝分裂末期细胞中的外部电场力线传导示意图;图6装置的架构示意图;图7A幅度调制单元的电路工作示意图;图7B方波形调制波示意图;图7C正弦波波形的载波示意图;图7D锯齿波调制的调幅波形态示意图;图8功率放大单元示意图;图9输出分配单元示意图;图10链条式绝缘电极固定支架未安装绝缘电极的整体示意图;图11链条式绝缘电极固定支架安装不同形状与大小的绝缘电极的整体示意图;图12绝缘电极底座结构示意图;图13绝缘电极结构示意图;图14绝缘电极安装于绝缘电极底座的示意图;图15多对绝缘电极交叉重叠病灶时绝缘电极对应位置示意图。
采用电场治疗主要基于细胞的生物电现象。生物电的产生一方面与细胞内外离子的不同分布有关,另一方面亦与细胞膜在不同状态下对离子选择性通透有关。细胞外液的正离子主要是Na+,负离子主要是Cl-,细胞内液的正离子主要是K+,膜对K+有较大的通透性,对Na+的通透性很差,对大分子有机物则不能透过,膜内的K+浓度比膜外高,故倾向于向膜外流出,但带负电荷的大分子有机物却不能随之向膜外流出,膜外高浓度的Na+也不能向膜内流入以与K+交换,因此,造成了膜内外电位差,膜外为正,膜内为负;由于离子浓度差膜内K+向膜外透出,由于电位差膜外K+倾向于向膜内透入,两者形成电-化学平衡时,K+向膜外透出与向膜内透入的速度相等,不再变化,此时的电位差即静息电位,膜的内外两侧分为两极的这种状态,称为极化状态,故活细胞膜是极化膜,由于膜的阻抗大膜内外一般没有电流通过。此时细胞内电场均一,就整个细胞而言,对外不显电性。当施加外部电场时,若细胞受到足够强度的刺激后(如电场或电流刺激),膜的通透性可立即发生改变,对Na+的通透性突然增加,膜外高浓度的Na+快速内流,导致暂时性的膜内电位等于或高于膜外电位,引起细胞膜的极化状态消失或逆转,细胞膜表面由原来的带正电荷的状态转为带负电,膜内侧由负电位转为正电位,这种膜内外电位差消失或反转的现象称为除极化,引起除极化的最小电场或电流强度称为阈强度值。但在单次刺激后的除极是一瞬间的过程,除极后立即恢复原来的极化状态,称为复极。除极现象可以通过电介质的极化理论来阐述。电介质可分为两类,一类是由无极分子组成(如细胞内的二氧化碳),在没有外电场作用时,由于每个分子的正、负电荷“重心”重合,偶极矩为零,此类介质的整体或任何一个局部都不显电性;但在外电场的作用时,每个分子的正、负电荷“重心”要向相反方向发生微小位移而不再重合,且偶极矩方向与电场方向一致,这种变化为位移极化,外电场愈强,分子正负电荷“重心”的相对位移愈大,介质被极化的程度就愈高,若撤去外电场,分子正负电荷“重心”又重合在一起,极化消失。另一类是由有极分子组成(如细胞内组成微管的管蛋白分子),在无外电场作用时,虽然每个分子的正负电荷“重心”不重合,偶极矩不为零,但由于介质中大量分子的无规则热运动,使分子偶极矩的方向杂乱无章,故介质的整体或任何一个局部也不显电性;但在外电场作用时,分子间电偶极矩要转向外电场方向;不过,由分子热运动的干扰,分子偶极矩又可能与外电场方向不完全一致,外电场愈强,分子偶极矩转向电场方向的程度就愈高,这种变化称为转向极化。
外电场对细胞有丝分裂的影响,可以通过电偶极分子在外电场中所受的力矩理论来阐述。细胞内的极性与非极性分子以及微管等细胞器均可视为偶极子。当外电场均匀时,如附图1A所示,偶极子轴线L与外电场E方向之间的夹角为Q,偶极子电荷+q、-q所受的力F+、F-大小相等,方向相反,整个偶极子所受合外力为零,但F+、F-的作用线不在一条直线上,它们组成一力偶,偶极子所受力偶矩(T)的大小为T=FLsinQ=qELsinQ,力偶矩的方向垂直纸面指向读者,可将P、E、T三者的大小与关系一起表示出来,即T=qL E=PE(E为电场、P为极化强度矢量),这个力偶矩将使偶极子转至与外电场相一致的方向,如图1B所示,当Q=0,即P与E平行时,T=0,偶极子达稳定平衡。当外电场不均匀时,偶极子正、负电荷所受电场力的大小和方向都不相同,因此偶极子除受力矩的作用外,还需受到一个不为零的合外力的作用,力矩使偶极子的偶极矩转至与外电场一致的方向,而合外力则使偶极子在外电场中沿场强较强的方向移动,如附图2A、图2B所示。
本发明的一种采用调幅电场治疗肿瘤装置的主要特征之一是在一对绝缘电极间产生强度连续交替变化的调幅电场,这种调幅电场为不均匀的电场。调幅电场是通过幅度调制单元调制的调幅波信号经功率放大单元放大后传导到绝缘电极而产生。调幅波是在幅度调制单元采用低频(或超低频)调制波对频率高于调制波的载波进行调制而成。调幅波的包络线波形与调制波波形相同,频率与载波相同,调幅波的幅度随载波与调制波幅度的矢量增减变化,如附图4为采用正弦波为调制波调制的调幅波的形态,调幅波经功率放大单元放大后施加到绝缘电极上,则在一对绝缘电极间产生强度随调幅波变化的调幅电场,调幅电场作为不均均的外电场施加到病灶区,一方面可干扰破坏细胞有丝分裂,同时这种强度连续交替变化的电场能确保肿瘤细胞遭受其敏感强度的电场刺激,因此适用于对肿瘤的治疗。当细胞处于分裂期时如附图3,其有丝分裂过程中有两个环节受外电场的影响较大。第一,是在细胞有丝分裂前期细胞内出现纺锤丝的环节。纺锤丝是由许多微管集聚而成,而微管又是由13根丝状蛋白质分子(管蛋白)所围成的中空纤维,集聚成纺锤丝的微管的结构是不稳定的,微管具有极强的偶极矩,对电场敏感。当有丝分裂前期的细胞在遭受不均匀的外电场时,细胞内的微管发生转向极化,一方面使微管由取向杂乱无章转至为与外部电场一致的方向排列;同时遭受合外力可使微管向场强较强的方向移动。这样造成微管不能聚集形成纺锤丝而中止细胞的有丝分裂。第二,是在细胞有丝分裂末期的细胞中部出现细胞膜深度凹陷(有丝分裂沟)的环节。在细胞中部细胞膜凹陷生成两个新细胞的过程中,越来越狭小的有丝分裂沟成为细胞质在两个未完全分开的亚细胞之间流动的通道。当施加的外电场力线与细胞分裂长轴方向平行时,如附图5所示,一方面电场力线从与电场正极较近的亚细胞穿过进入分裂细胞,然而它们并不从有丝分裂沟处的细胞膜流出,而是在与正极较近的亚细胞中畸变传导后在有丝分裂沟处汇聚,使有丝分裂沟处的电场力线密度显著提高;另一方面与前所述的微管等由有极分子组成的细胞质发生转向极化后向着场强较强的有丝分裂沟处移动,使两个亚细胞内由有极分子组成的细胞质移动汇集在有丝分裂沟处,在库仑力作用下,细胞质发生随外电场强度与频率不同的振动使有丝分裂沟处的细胞膜承受更大并具有“锤击”效应的力而发生破裂。
附图6是本发明的一种采用调幅电场治疗肿瘤装置的架构示意图,包括以下功能单元:中央控制单元1、调频信号发生单元2、电源单元3、幅度调制单元4、功率放大单元5、输出分配单元6、以及绝缘电极7组成。调频信号发生单元2采用直接数字频率合成器或由变容二极管组成的调频电路、幅度调制单元4采用晶体管调幅电路或集成电路调幅电路、功率放大单元5采用中频功率放大电路、输出分配单元6采用分配控制电路和电子开关来实施。中央控制单元1采用微型触屏工业平板电脑、或单片机、或PC电脑或者手机终端措施;中央控制单元还包括人机交互单元。
中央控制单元1按设定参数控制调频信号发生单元2产生某一频率固定,或频率在一定范围内变化的波形信号,该频率波形信号作为载波输入幅度调制单元4。
如附图7A所示,中央控制单元按设定参数控制幅度调制单元4,以锯齿波形如附图7B的低频信号作为调制波,将附图7C正弦波形的载波调制成调幅波如附图7D,调幅波的包络线波形与调制波的波形相同,其频率与载波频率相同,其幅度随载波与调制波的幅度矢量加减而变化,最终在每对绝缘电极间产生电场强度随调幅波发生相应变化的调幅电场。
如附图8所示,上述调幅波从功率放大单元5的导线11输入,放大倍数由中央控制单元1控制,放大后由导线12输出到输出分配单元6的导线16。如图9所示,中央控制单元1根据需要通过控制输出分配单元6的17控制内部的电子开关,将调幅波分配给一对绝缘电极18、19或多对绝缘电极。
链条式绝缘电极固定支架如图10、图11所示,绝缘电极的固定支架20为柔性绝缘材料制造,长度可以根据需要增加或减少链条节数任意改变,两端由弹性材料制造,围绕在人体的任何部位都可紧贴人体;链条式绝缘电极固定支架固定绝缘电极的底座21,安装绝缘电极后的绝缘电极底座22。图12为绝缘电极底座结构示意图,底座壳体28,绝缘材料制作,上安装槽29,下安装槽30。
图13为绝缘电极结构示意图,绝缘电极本体23,其结构是在导电材料表面涂敷高强度绝缘层,可根据需要做成不同形状和大小;扣式导线连接点24,通过导线与输出分配单元6的对应输出接口相连,绝缘电极连接导线的这一面朝外不与人体接触;下固定桩25、上固定桩26,均为绝缘材料制作,安置到绝缘电极底座上时卡入图10的下安装槽30;上固定桩26安置到绝缘电极底座上时卡入图10的上安装槽29,弹簧27使上固定桩26和下固定桩25紧紧顶住绝缘电极底座内的上安装槽29和下安装槽30,但可以绕上固定桩25和下固定桩26形成的轴转动,如图14,使用时,安装槽开口一侧朝向人体。
图11为链条式绝缘电极固定支架整体示意图,绝缘电极安装位置由适形模态计划系统根据影像信息确定,可精确定位每对绝缘电极的电场,使其均覆盖肿瘤病灶区。
图15为多电场交叉覆盖肿瘤病灶时绝缘电极对应位置示意图,每对绝缘电极呈不同的方向分布,高电位绝缘电极,例如绝缘电极A1、B1、C1、D1固定在人体的一侧,低电位绝缘电极,例如绝缘电极A0、B0、C0、D0固定在人体的另一侧,可防止多对绝缘电极同时工作的模式下绝缘电极之间的相互影响。如果有n对绝缘电极轮流工作一次,每对绝缘电极产生的外电场都覆盖了肿瘤病灶区,肿瘤病灶区承受了n次外电场作用,增加了对肿瘤病灶区的作用强度,而电场覆盖区的正常细胞只承受了一次外电场作用,减少了对正常细胞的损伤。
实验一:比较绝缘电极间强度以文献报导的敏感强度为中间值的连续交替变化的外电场与绝缘电极间强度固定为文献报导敏感强度的外电场对葡萄膜黑色素瘤的抑制作用。葡萄膜黑色素瘤具有较高的增殖性,显著的耐药性,文献报导恶性黑色素瘤敏感电场强度为1.4V/cm,适用于破坏黑色素瘤细胞的电场频率为120KHZ。
接上所述,癌细胞混悬液的制备方法:取刚摘除的葡萄膜黑色素患者眼球,从瘤体表面及基底部取出新鲜的肿瘤组织,剪成细块在200目的不锈钢筛网上研磨到培养液中,每分钟1000转离心10分钟,弃去上清液,培养基吹匀,取5毫升接种于50毫升培养瓶中,5%二氧化碳培养箱中37℃孵育24小时,去除团块状的半量换液后,继续培养24小时,再同法半量换液后的培养物即为所需的癌细胞混悬液。
接上所述,癌细胞混悬溶液中每1升中含癌细胞个数的计数方法:将癌细胞混悬溶液稀释到不同稀释级数,精密量取不同稀释级数的混悬溶液200微升置盖玻片上(盖玻片的大小与形状相同),均匀分布后用100微升注射器滴加1滴10%甲醛生理盐水及1滴丙酮,原位固定,采用肿瘤特异性HMB45抗体免疫组织化学染色。在不同位置选取10个视野,计数HMB45阳性细胞。视野中HMB45阳性细胞的特征:癌细胞的细胞质中有均匀分布的红色阳性产物,癌细胞呈梭形或上皮形生长。培养液采用美国GIBCO公司生产的DMEM/F12(1:1)干粉培养基配制。
接上所述,试验方法:取编号为1号、2号、3号正方形培养瓶,1号培养瓶抵靠瓶的四壁安装两对绝缘的绝缘电极对A1与绝缘电极对A2,两对绝缘电极频率均为120KHZ,电场强度均为1V/cm~3V/cm之间的连续交替变化;2号培养瓶抵靠瓶的四壁安装两对绝缘的绝缘电极对B1与绝缘电极对B2,两对绝缘电极频率均为120HZ,两对绝缘电极间的电场强度均为1.4V/cm;绝缘电极对A1与绝缘电极对A2交替使用,绝缘电极对B1与绝缘电极对B2交替使用,每对绝缘电极交替使用时间均为30秒。1号、2号、3号培养瓶各精密加入培养液45毫升,再分别精密加入每1升含1~9×106个癌细胞混悬液5毫升,1号、2号3号培养瓶同时置5%二氧化碳培养箱37℃孵育48小时,然后进行培养物的癌细胞计数。
接上所述,试验结果:向培养瓶中加入的癌细胞混悬液的浓度是每1升含癌细胞个数为8.6×106个;三个培养瓶中加入5毫升上述癌细胞混悬液后每1升含癌细胞个数为86×104个;培养48小时后,1号瓶培养每1升癌细胞混悬液含癌细胞为8×104个,2号培养瓶每1升含癌细胞个数为每1升25×104个,3号培养瓶每1升含癌细胞个数为218×104个;绝缘电极间电场强度在1V/cm~3V/cm范围连续交替变化的外电场对葡萄膜黑色素瘤增殖抑制率为90.7%,绝缘电极间电场强度固定为1.4V/cm的外电场对葡萄膜黑色素瘤增殖抑制率为70.9%,即绝缘电极间强度在1V/cm~3V/cm范围连续交替变化的外电场对癌细胞增殖的抑制率高于绝缘电极间场电强度固定在1.4V/cm的外电场对癌细胞增殖的抑制率。试验结果说明,不均匀的外电场对覆盖区的大多数癌细胞有效,而均匀的外电场仅对分裂细胞长轴与外部电场力线方向平行的分裂细胞有效,也就是如前所述,不均匀的外电场的作用机制是双重的,而均匀的外电场的作用机制是单一的。
实验二:比较绝缘电极间强度以文献报导的敏感强度为中间值的连续交替变化的外电场与绝缘电极间强度固定为文献报导敏感强度的外电场对神经胶质母细胞瘤的抑制作用。文献报导对神经胶质母细胞瘤抑制最强的电场强度为2.5V/cm,适用于破坏神经胶质母细胞瘤的电场频率为200KHZ。
接上所述,细胞培养方法:取刚手术吸取的多形性胶质母细胞瘤组织,在半小时内机械离散后接种于培养瓶内,加入含15%胎牛血的培养液,5%二氧化碳培养箱中37℃孵育,约一周后细胞长满瓶壁,分装传代。培养液采用美国GIBCO公司生产的DMEM干粉培养基配制。
接上所述,集落形式试验:将指数期生长细胞分别接种于1号方形培养瓶、2号方形培养瓶、3号方形培养瓶中,每瓶4万细胞。1号培养瓶抵靠瓶的四壁安装两对绝缘电极对A1与绝缘电极对A2,两对绝缘电极频率均为200KHZ,电场强度均在2V/cm~4V/cm之间连续交替变化;2号培养瓶抵靠瓶的四壁安装两对绝缘电极对B1与绝缘电极对B2,两对绝缘电极频率均为200HZ,两对绝缘电极间的电场强度均为2.5V/cm;绝缘电极对A1与绝缘电极对A2交替使用,绝缘电极对B1与绝缘电极对B2交替使用,每对绝缘电极交替使用时间均为30秒。1号、2号、3号培养瓶同时开始培养,一周后换液,二周后用Carnoy固定液(上海歌凡生物科技有限公司生产)固定,吉姆萨染剂染色,计数所形成的30个细胞以上的集落,计算癌细胞存活率。
按上所述,试验结果:1号培养瓶集落数352,2号培养瓶集落数765,3号培养瓶集落数1498,以3号培养瓶集落数为基础,计算1号培养瓶、2号培养瓶的癌细胞增殖的抑制率:1号培养瓶为76.5%,2号培养瓶为48.9%,即绝缘电极间以强度2.5V/cm为中间值的连续交替变化的外电场对癌细胞增殖的抑制率高于绝缘电极间电场强度固定在2.5V/cm的外电场对癌细胞增殖的抑制率。试验结果说明,不均匀的外电场对覆盖区的大多数癌细胞有效,而均匀的外电场仅对分裂细胞长轴与外部电场力线方向平行的分裂细胞有效,也就是如前所述,不均匀的外电场的作用机制是双重的,而均匀的外电场的作用机制是单一的。
实验三:比较不同电场强度对葡萄膜黑色素瘤增殖的抑制作用。采用上所述的实验一的方法。文献报导的恶性黑色素瘤的敏感电场强度为1.4V/cm,为此采用四个培养瓶进行平行试验,1号培养瓶施加的电场强度为1.0V/cm,2号培养瓶施加的电场强度为1.4V/cm,3号培养瓶施加的电场强度为3.0V/cm,电场频率均为120KHZ,4号培养瓶不施加外部电场作为对照。
按上所述,试验结果:向各培养瓶加入的癌细胞混悬液的浓度是每1升含癌细胞数为9.2×106个,每个培养瓶加入5ml后,瓶内50ml培养液含癌细胞个数为92×104个;培养48小时后,瓶内培养液每1升含癌细胞个数:1号瓶为54×104个,2号培养瓶为26×104个,3号培养瓶为28×104个,4号培养瓶为231×104个;癌细胞增殖抑制率:1号培养瓶为41.3%,2号培养瓶为71.7%,3号培养瓶为69.6%。试验结果表明,葡萄膜黑色素瘤存在敏感电场强度,其敏感电场强度为1.4V/cm左右,电场强度对癌细胞增殖影响较大。另外试验结果也提示,临床应用时要准确确定不同环境下的癌细胞的敏感电场强度以及如何界定治疗时癌细胞实际遭受的电场强度是不是其敏感的电场强度,都是困难的,因此以文献报导或体外试验得到的癌细胞敏感电场强度为中间值的一定范围内强度连续交替变化的调幅电场用于肿瘤治疗,是确保癌细胞遭受敏感电场强度刺激的最有效的方法。
- 还没有人留言评论。精彩留言会获得点赞!