一种普鲁士蓝/三氧化钨复合光催化剂及其制备方法与应用与流程
本发明属于环境保护技术领域,涉及一种光催化剂的制备方法,具体涉及一种采用先简单化学沉积而后溶剂热制备PB/WO3复合光催化剂的方法。
背景技术:
随着工业化进程的不断加剧,水体污染成为当今社会亟待解决的问题之一。异质光催化作为一种有效技术,可以利用太阳光辐照,在催化剂存在下,对有机物进行深度氧化,节约能源而且不污染环境,因而具有很大的应用前景。
我国钨资源蕴藏量丰富,居世界第一,因而WO3的来源相对广泛。作为一种n型半导体,其带隙能为2.4-2.8eV,能响应460-500 nm的可见光,是一种可见光响应型光催化剂。近年来在光化学、光催化剂、光致发光、气敏性等应用领域引起了广泛关注。大量对于WO3微纳米结构的研究均表明该半导体在降解有机化合物方面展现了良好的光催化活性。但对于该单一体系,仍然存在下述几个需要解决的问题:一是其吸收阈值仅约470 nm,对太阳能的利用率仍然较低;二是WO3的导带位置约0.5~0.7V相对O2/O2-·的电势(-0.046V)偏正,不利于氧气的单电子还原,导致半导体中光生电子-空穴的复合速率很快,使光量子效率相对较低。这两个问题的存在使WO3光催化活性的进一步提高受到限制。因此,拓宽WO3的可见光响应范围,促进光生电子-空穴的有效分离与转移,是目前该催化剂研究中需要解决的关键问题。
过氧化氢(H2O2)与二价铁离子的混合溶液组成的芬顿试剂在氧化过程中产生强氧化剂 ·OH,可降解包括染料在内的多种有机物,因而被广泛应用于有害有机物的处理。然而传统芬顿技术只能在酸性条件下进行,当pH较高时Fe2+易生成沉淀,产生的铁泥会造成二次污染,增加处理成本,同时会抑制·OH生成,终止芬顿反应,限制其应用和推广。因此,寻找有利于改善芬顿反应条件的铁负载催化剂成为当前的研究热点。普鲁士蓝的化学式组成为Fe4[Fe(CN)6]3,其组成中既有Fe2+又有Fe3+,其中,Fe3+/Fe2+的标准电极电势为0.771V,比WO3导带的电势(0.5~0.7V)更正,因此Fe3+能够捕获WO3导带上的电子,从而使WO3的光生电子和空穴得到有效分离;同时形成的Fe2+又能被加入的H2O2氧化成Fe3+ ,从而实现了离子之间的循环转化,构成一个类芬顿反应。
基于上述思路,我们设计了WO3与普鲁士复合光催化剂,并从节约能源、保护环境的角度出发,探索了一种操作简单、成本低廉且高效的新型复合光催化剂,具有重要的理论和实际意义。
本发明本着简化制备工艺、节约能源并提高性能的角度,通过简单化学沉积而后溶剂热的方法实现了PB和WO3半导体的复合,发现PB与WO3 的摩尔比在0.0005:1~0.1:1的范围内光催化活性均明显提高,其中摩尔比为0.03:1时的光催化活性最佳,其动力学常数为0.4546min-1,达到纯WO3样品的19.0倍。
技术实现要素:
为实现上述目的,本发明公开了一种普鲁士蓝PB/WO3复合光催化剂,其特征在于它是由PB与WO3组成;其中PB与WO3 的摩尔比为0.001:1~0.05:1;所述复合光催化剂中PB指的是摩尔比为3:4的K4Fe(CN)6·3H2O和FeCl3反应得到的产物;WO3指的是三氧化钨。其中最佳的PB与WO3 的摩尔比为0.03:1。
本发明进一步公开了普鲁士蓝PB/WO3复合光催化剂的制备方法,其特征在于按如下步骤进行:
称取一定量的Na2WO4·2H2O于25mL的聚四氟乙烯反应釜内衬中,加入5mL乙醇,磁力搅拌15min,将2mlNaCl溶液滴加于反应釜中,继续磁力搅拌15min,然后将5mL 1.5×10-6~1.5×10-4mol/L的K4Fe(CN)6·3H2O和5ml 2.0×10-6~2.0×10-4mol/L的FeCl3水溶液缓慢滴入上述混合溶液中,搅拌10-15min加入3M HCl调溶液pH为0.5~2.0,继续搅拌20~40 min后于60~200℃恒温反应2~12h,待冷却至室温后,将沉淀离心分离、洗涤、60℃干燥,收集所得粉末得到系列不同复合比例的 PB/WO3 复合光催化剂,所述的复合光催化剂中PB与WO3摩尔比在0.001:1~0.05:1。优选PB和WO3摩尔比在0.03:1。 本发明的制备方法中醇水体积比例为1:2.4,反应温度为100-120℃。
本发明更进一步公开了普鲁士蓝PB/WO3复合光催化剂在降解有机染料方面的应用。其中的降解有机染料指的是降解印染和造纸车间排污水中所含难降解性芳香类化合物方面的应用。该复合光催化剂在降解有机染料方面表现出良好的催化性能。所采用的制备方法为简单化学沉积而后醇-水混合溶剂热法,所得样品具有优异的光催化性能,这些优势预示着该光催化剂在工业废水处理领域的良好应用前景。
附图说明:
对所得部分光催化剂的结构、性能表征结果如下:
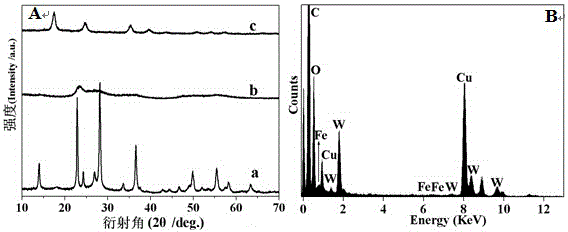
图1为不同样品的XRD、EDS图谱;其中A为系列不同样品的XRD图谱:(a) WO3;(b) PB/WO3 -0.03;(c) PB;显然相比于纯WO3,复合光催化剂的衍射峰相当低,说明复合光催化剂的结晶度较差,不容易通过该表征清楚地检测WO3和PB的存在。因此进一步对样品进行了电子能谱(EDX)的表征,如图1B所示,除了WO3中的W和O两种元素外,从能谱图中清楚检测到了普鲁士蓝中Fe元素的存在,表明产物为普鲁士蓝与WO3形成的复合光催化剂;B为PB/WO3 -0.03复合光催化剂的EDS图谱;
图2为 WO3、PB及PB/WO3不同复合比例的紫外-可见漫反射光谱; WO3陡峭的吸收光谱形状说明其来自本征带隙跃迁,虽然在可见光区也表现出一定的吸收,但由于其带隙能约2.64eV,因此吸收带边仅约470 nm,对可见光区的吸收仍相对较少。而PB的吸收光谱范围很宽,在200-800 nm的整个紫外-可见波段都有较强吸收。当将PB和WO3复合后,PB/WO3复合光催化剂的吸收带边明显红移。而且随着PB复合比例的增加,材料在可见光区的吸收程度也有所增强。紫外-可见漫反射光谱表明PB的复合有效拓宽了WO3对可见光的吸收,从而能够更加有效地利用太阳能;
图3为在410nm紫外光激发下PB复合前后的WO3荧光光谱;荧光光谱常用来考察半导体中光生载流子的迁移和复合过程,荧光强度的减弱意味着载流子的复合几率降低。WO3在500-580 nm表现出较宽的黄绿色荧光发射带,其中525 nm的最强荧光峰归属于激发电子从导带的跃迁回价带,从而引起光生电子-空穴复合而释放出的能量。WO3经复合PB之后,荧光峰形与复合前基本一致,但荧光强度有所下降,尤其PB/WO3-0.03样品的峰强度降低明显,说明PB的复合可有效抑制电子-空穴的复合。但PB与WO3摩尔比过高(0.05:1)时,复合光催化剂的荧光强度反而又增强,这是由于过高的PB含量意味着在材料中引入了过多的相缺陷,而其又可成为光生载流子的复合中心。因此,在一定的复合比例内,PB的复合可有效抑制WO3中光生电子与空穴的结合几率,从而提高光量子效率。
图4 为5 mg不同复合比例PB/WO3光催化剂在500W Xe灯辐照下,光催化降解10 ml 10-5 M的MO溶液的性能对比图;其中(a)降解效率;(b)光催化反应速率常数;空白实验表明MO在无光催化剂存在的情况下,经10min辐照后,仅有约1.2%的MO发生了降解,说明光照的影响可以忽略;WO3对染料分子的吸附很少,也不影响系列光催化剂的性能对比。在过氧化氢的协同下比较系列WO3基光催化剂的性能可以看出, 复合PB后WO3的光催化剂,活性均明显提高,且表现出随着PB元素复合比例的提高,催化降解效率先是大幅度提高,而后又稍有降低的趋势,但均明显优于未经复合的WO3。在纯WO3存在下,光照10min后对MO的降解率为22.7%;PB/WO3-0.01的样品在光照10min后对MO的降解率大幅增长至74.1%;而当PB/WO3摩尔比增大为0.03:1时,经过同样的辐照时间,MO的吸光度几乎降为零,表明染料已基本被降解完全。进一步增大PB与WO3的摩尔比为0.04:1时,同等时间内MO的降解率为83.3%。根据准一级反应动力学(图4b),纯WO3的降解反应速率常数为0.02386 min-1,而PB/WO3-0.03的速率常数为0.4546 min-1,是复合前样品的19.0倍,显示出最佳光催化活性。因此选定PB/WO3摩尔比为0.03:1为最佳复合比例。
具体实施方式:
为了进一步解释本发明,提供下述制备方法实施实例。以下实施例的表述不限制本发明,本领域的专业人员可按照本发明的精神对其进行改进和变化,所述的这些改进和变化都应视为在本发明新型的范围内。本发明所述的各种原料例如Na2WO4·2H2O、NaCl、HCl均有市售。
实施例1
称取一定量的Na2WO4·2H2O于25ml的聚四氟乙烯反应釜内衬中,加入5mL乙醇,磁力搅拌10 min,将2ml NaCl溶液滴加于反应釜中,继续磁力搅拌15min,然后将5ml 1.5×10-6mol/L的K4Fe(CN)6·3H2O和5ml 2.0×10-6mol/L的FeCl3溶液缓慢滴入上述混合溶液中,搅拌10min后,加入3MHCl调溶液的pH约为1,继续搅拌20 min后于100℃恒温反应4h,待冷却至室温后,将沉淀离心分离、洗涤、60℃干燥,即可得到摩尔比为0.001:1的PB/WO3光催化剂。
实施例2
称取一定量的Na2WO4·2H2O于25ml的聚四氟乙烯反应釜内衬中,加入5mL乙醇,磁力搅拌12min,将2mlNaCl溶液滴加于反应釜中,继续磁力搅拌15min,然后将5ml 4.5×10-5 mol/L的K4Fe(CN)6·3H2O和5ml 6.0×10-5 mol/L的FeCl3溶液缓慢滴入上述混合溶液中,搅拌12min后,加入3MHCl调溶液的pH约为0.5,继续搅拌30 min后于100℃恒温反应4h,待冷却至室温后,将沉淀离心分离、洗涤、60℃干燥,即可得到摩尔比为0.03:1的PB/WO3光催化剂。
实施例3
称取一定量的Na2WO4·2H2O于25ml的聚四氟乙烯反应釜内衬中,加入5mL乙醇,磁力搅拌15min,将2mlNaCl溶液滴加于反应釜中,继续磁力搅拌15min,然后将5ml 7.5×10-5 mol/L的K4Fe(CN)6·3H2O和5ml 1.0×10-4mol/L的FeCl3溶液缓慢滴入上述混合溶液中,搅拌15min后,加入3MHCl调溶液的pH约为1.5,继续搅拌40 min后于100℃恒温反应4h,待冷却至室温后,将沉淀离心分离、洗涤、60℃干燥,即可得到摩尔比为0.05:1的PB/WO3光催化剂。
实施例4
印染车间所排污水中含有的难降解性芳香类化合物的降解实例:
甲基橙是印染工业常用的难降解芳香类橙色染料,从印染车间取含有甲基橙染料3.27mg/L的废水500mL,加入PB与WO3摩尔比为0.03:1的PB/WO3光催化剂250 mg,再滴入一定量的过氧化氢,在XPA-7型光化学反应仪暗箱中磁力搅拌达到吸-脱附平衡,经500W氙灯模拟日光辐照10 min后,立即过滤分离,测上清液吸光度计算MO的降解率为99.5%,而同等条件下纯WO3的光催化降解效率仅为22.7%。
实施例3
选定性能最佳的PB/WO3 0.03:1样品,对除甲基橙外的其它染料,包括橙黄和丽春红也分别进行了相同条件下的光降解实验,并和未经复合的WO3样品进行了对比,所得数据列表如下:
从上表数据可以看出,PB/WO3-0.03不但对甲基橙的降解效率明显高于未经复合的WO3,对染料橙黄和丽春红的降解表现出同样的优势。说明该发明中的复合光催化剂在降解印染车间所排含难降解性芳香类化合物的污水中确实具有良好的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!