电解液、电池和电池组的制作方法
本发明涉及一种用于电池的电解液,以及利用该电解液的电池。
背景技术:
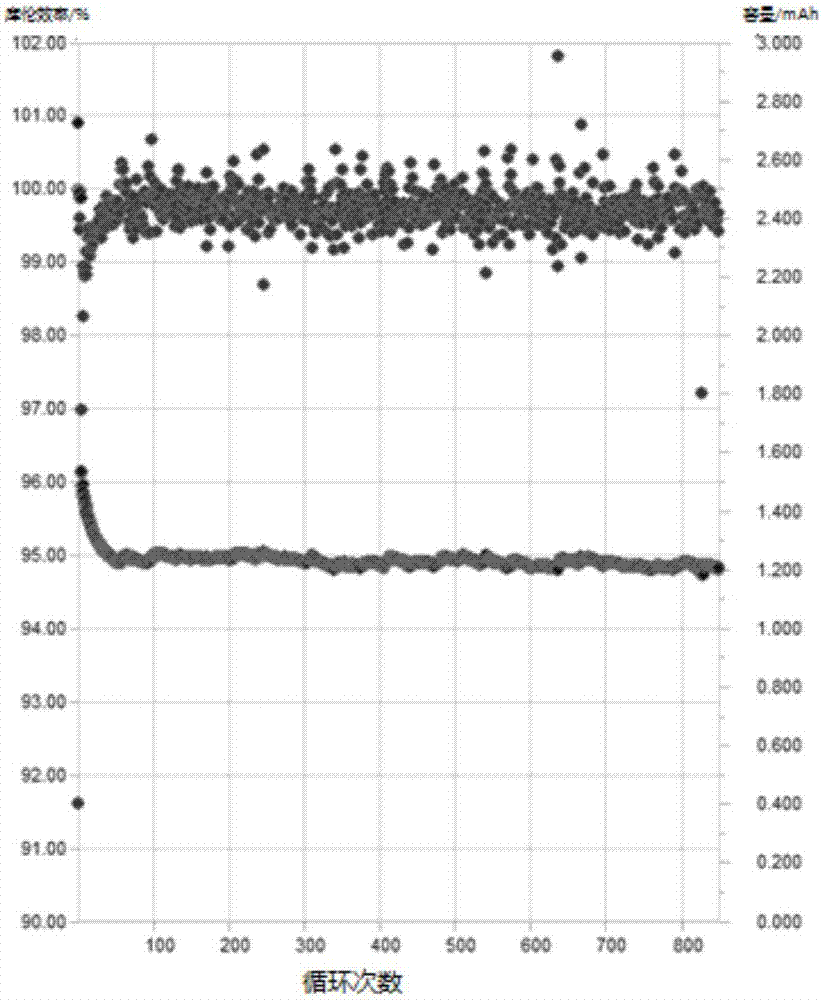
:铅酸电池,其出现已超百年,拥有着成熟的电池技术,占据着汽车启动电瓶、电动自行车、ups等储能领域的绝对市场份额。铅酸电池虽然循环使用寿命较低,能量密度也相对较低,但却拥有价格非常低廉,性价比非常高的优点。因此,近些年来,镍氢电池、锂离子电池、钠硫电池、液流电池等,均无法在储能领域取代铅酸电池。近几年来出现一种新型水系二次电池。该二次电池的正极能够基于金属离子进行可逆的脱出-嵌入反应,负极能够基于金属离子进行可逆的还原沉积-氧化溶解反应,电解液含有参与正极脱出-嵌入反应的金属离子和参与负极沉积-溶解反应的金属离子。该类型电池的电解液为水溶液,不存在类似锂离子电池中有机电解液的安全隐患,且对环境友好,成本较低,能量密度高。因此,该类型电池非常有希望成为替代铅酸电池的下一代储能电池,具有极大的应用价值。该类型电池的参与负极沉积-溶解反应的金属离子可以为锌离子,此时负极活性物质为金属锌,然而这类负极活性物质在水溶液中充放电时存在枝晶、腐蚀、析氢等问题,从而使电池的循环性能、充放电容量受到影响。因此,现有技术需要进一步改善。技术实现要素:虽然已经尝试了多种电解液的添加剂,但是对于现有的电池来说,目前的添加剂仍然存在无法充分地解决负极活性物质在水系溶液中的枝晶、腐蚀、析氢等问题。鉴于现有技术中存在的技术问题,本发明的目的是提供一种能够用于电池的电解液,该电解液可以有效地抑制负极,尤其是锌负极的枝晶、腐蚀、析氢等问题。本发明提供一种电池用电解液,所述电解液包括充放电过程中在负极能够还原沉积为金属且该金属能可逆氧化溶解的负极金属离子;参与电池正极反应的正极离子;以及添加剂离子,所述添加剂离子选自na、mg、al、nh4+、ni、co、ce、fe、pb或mn离子中的至少一种,并且所述添加剂离子不同于负极金属离子和正极离子。优选的,添加剂离子在电解液中的浓度为0.001m~8m。优选的,添加剂离子mg离子在电解液中的浓度为0.001m~0.5m。优选的,添加剂离子ce、fe、mn、pb和/或co离子在电解液中的浓度为0.1m~8m。优选的,所述负极金属离子为锌离子。优选的,所述正极离子选自锂离子、钠离子或者镁离子。优选的,所述负极金属离子为锌离子,所述正极离子为溴离子或钒离子。优选的,所述电解液的ph为2~8。优选的,所述电解液还包括溶剂,所述溶剂为水和/或醇。本发明还一种电池,所述电池包括:正极、负极以及所述的电解液。本发明还提供一种电池组,包括若干个电池,电池如前所述。根据本发明,电池的循环性能、充放电容量获得了进一步的提升,此外,使用了本发明的电解液的电池,具有良好的容量保持率,放电电容损失低,并且能够实现深度放电。通过在电解液中添加给定的添加剂离子或者添加给定浓度的给定添加剂离子,采用这种新的电解液可以有效地抑制负极(例如锌负极)的枝晶、腐蚀、析氢等问题,从而获得电池循环性能,充放电容量得到提高,并意外地发现能够实现电池的深度放电。附图说明图1-3是电池b1、b3和b4的充放电循环性能图;图4是电池b5在0.2c倍率下的充放电曲线;图5是电池b5在0.2c倍率下在0.5~2.1v电压区间内的充放电曲线;图6是电池b5在3c倍率下的充放电循环性能图;图7是电池s1在3c倍率下的充放电循环性能图。具体实施方式下面结合具体实施方式对本发明进行详细的说明。在一个方面中,本发明提供一种电解液,其包括电解质和溶剂;其中所述电解质包括:充放电过程中在负极能够还原沉积为金属且该金属能可逆氧化溶解的负极金属离子;参与正极反应的正极离子;以及添加剂离子,所述添加剂离子选自na、mg、al、nh4+、ni、co、ce、fe、pb或mn离子中的至少一种,并且所述添加剂离子不同于上述负极金属离子和正极离子。在一个方面中,本发明的添加剂离子在电解液中的浓度为0.001m~8m(mol/l)。作为添加剂离子的所述al离子在电解液中的浓度为0.001m~8m(mol/l),优选为0.01m~5m,进一步优选0.1m~2m。作为添加剂离子的所述na、mg和/或ni在电解液中的浓度为0.001m以上且小于1m,优选为0.5m以下,更优选0.3m以下,更优选0.2m以下,更优选0.1m以下,更优选0.09m以下,更优选0.08m以下,更优选0.07m以下,更优选0.06m以下,更优选0.05m以下,以及优选0.001m以上,优选0.005m以上,优选0.01m以上。作为添加剂离子的所述ce、fe、mn、pb和/或co在电解液中的浓度为大于0.1m且8m以下,优选在0.2m以上,更优选在0.3m以上,更优选在0.4m以上,更优选在0.5m以上,更优选在0.8m以上,且优选在8m以下,更优选在5m以下,更优选在2m以下。作为添加剂离子的所述nh4+离子在电解液中的浓度为0.25m以上且8m以下,优选为0.25~4m,进一步优选为0.5~2m。当添加剂离子采用na、mg、k或ni时,此时的正极离子和负极金属离子与添加剂离子不同,即均不选自na、mg、k和/或ni。当添加剂离子采用ce、fe、mn、pb或co时,此时的正极离子和负极金属离子与添加剂离子不同,即均不选自ce、fe、mn、pb和/或co。此外,在本发明中作为添加剂离子在电解液中的浓度是指当该离子作为添加剂离子时在电解液中的浓度。此外,如果使用上述两种或两种以上添加剂离子时,上述浓度是指每种添加剂离子各自的浓度。添加剂离子来源于向电解液中添加的无机添加剂,无机添加剂选自钠化合物、镁化合物、铝化合物、铵化合物、镍化合物、钴化合物、铈化合物、铁化合物、铅化合物以及锰化合物中的一种或者两种或者更多。在本发明中采用溶剂的目的是用来溶解包括负极金属离子,正极离子、以及添加剂离子在内的电解质成分,并使得电解质在溶剂中电离,最终在电解液中生成可自由移动的阳离子和阴离子。本发明的溶剂优选为水和/或醇。其中醇包括但不限于甲醇或乙醇。电解液中的负极金属离子,在充放电过程中在负极能够还原沉积为金属,放电过程中该金属可逆氧化为金属离子。即在电池充电时,电解液中的负极金属离子还原成金属,沉积在负极上;在电池放电时,该金属氧化成为金属离子并从负极上溶出,进入电解液。优选地,负极金属离子为锌离子。负极金属离子在电解液中的浓度范围为0.5-15m。负极金属离子以氯酸盐、硫酸盐、硝酸盐、醋酸盐、甲酸盐、磷酸盐等形式存在于电解液中。优选,负极金属离子以硫酸盐、醋酸盐或硫酸盐和醋酸盐的混合物的形式存在于电解液中。电解液还包括参与正极反应的正极离子。该正极离子可以是在电池正极发生嵌入和脱出的金属离子或在充放电过程中参与正极氧化还原反应的离子。在本发明的实施方式一中,该正极离子是在电池正极发生嵌入和脱出的金属离子。在电池充电时,电解液中的该正极离子嵌入到正极材料中;电池放电时,充电时嵌入的该离子又从正极材料中脱出到电解液中。优选地,正极离子为锂离子。此时,正极离子在电解液中的浓度范围为0.1-30m。该正极离子以氯酸盐、硫酸盐、硝酸盐、醋酸盐、甲酸盐、磷酸盐等形式存在于电解液中。优选的,正极离子以硫酸盐、醋酸盐或硫酸盐和醋酸盐的混合物的形式存在于电解液中。在本发明的实施方式二中,该正极离子是在充放电过程中参与正极氧化还原反应的离子。在电池充电时,电解液中的该离子被氧化;电池放电时,充电时被氧化的活性物质又被还原。正极离子选自溴离子、钒离子中的一种或者两种。此时,当正极离子是溴离子的时候,其浓度可以为例如0.5m~20m。在一优选的实施方式中,电解液中包括锌离子和锂离子。随着充放电的进行,锌离子在负极发生沉积-溶解,锂离子在正极发生嵌入-脱出。在一优选的实施方式中,电解液中包括溴离子和锌离子,随着充放电的进行,锌离子在负极发生沉积-溶解,溴离子在正极发生氧化-还原反应。而在本发明中,通过在上述浓度范围内添加特定的添加剂离子,可以显著地抑制负极金属离子(例如锌离子)在水溶液中充放电时存在的枝晶、腐蚀以及析氢等问题,从而显著地改善了电池的循环性能和充放电容量,并意外地发现了还可以实现电池的深度放电。具体来说,通过在上述给定浓度范围添加给定的添加剂离子,可以显著地提高电池的开路电压和容量保持率,放电容量损失减小到未添加给定的添加剂离子的电池的70%左右。此外,在50个循环、100个循环和150个循环之后的容量保持率均可以保持在较高的水平,尤其是150个循环后的容量保持率显著高于不使用添加剂的情况,使得循环保持率可以始终保持在约95%以上。此外,在高库伦倍率的情况下,当循环稳定后,会保持数百个循环(超过1000个循环)其放电容量均非常稳定,波动小于5%,即容量保持率始终在95%左右。而未添加添加剂的情况在300个循环后,放电容量仅为初始放电容量的80%左右。说明添加了本发明的添加剂离子,蓄电池的循环寿命与稳定性得到大幅提高。本发明人通过观察电池的内部结构发现,由于添加剂了本发明的添加剂离子,在下述实施例的蓄电池中,直到电池进行充放电800个循环之前,均未出现在负极的枝晶的现象,而在未添加这样的添加剂离子的对比例中,通常在100~300个充放电循环的过程中就会出现在锌负极的枝晶,从而严重影响的容量。可见,采用了本发明的电解液制备的电池,其负极的腐蚀、析氢和枝晶等不良反应得到了良好地抑制,从而解决了本领域难以解决的问题,改善了电池的循环性能和充放电容量。此外,利用本发明的电解液时,还意外地发现可以实现电池的深度放电,通常采用本发明中涉及的电池(如下所述)时,通常仅可以放电到例如1.4v左右,而通过采用本发明的上述电解液,可以实现深度放电,放电到0.5v左右。推测这也是由于抑制了负极的腐蚀、析氢和枝晶等问题而带来的显著的效果。优选本发明电解液中的添加剂离子为镁离子或锰离子中的一种或者两种。优选地,提供镁离子或锰离子的无机添加剂选自它们各自的氧化物、醋酸盐、碳酸盐、硫酸盐、硝酸盐中的一种或者几种。在一优选的实施方式中,镁化合物为硫酸镁,锰化合物为硫酸锰。采用镁离子或锰离子的电解液与其他的添加剂离子相比,可以更进一步改善电池的循环性能和充放电容量,并可以实现电池的深度放电。无机添加剂加入电解液的方法,根据电解液或隔膜的不同情况,可以选择不同的加入方式。加入方式包括但不限于直接加入电解液中,或者以悬浮液滴加在隔膜上。更优选地,将无机添加剂直接加入到电解液中,然后将电解液滴到隔膜上。为了使电池性能更加的优化,在本发明的实施方式一或二中,本发明的电解液ph值范围优选3~7。ph的范围可以通过缓冲剂来调节。电解液的ph过高,可能会影响电解液中锌离子的浓度,电解液的ph过低,则会加剧电极材料的腐蚀。而将电解液的ph范围保持在3~7,既可以有效保证电解液中各种离子的浓度,还可以避免电解腐蚀。本发明还涉及一种电池,其包括正极、负极和上述电解液。本发明的实施方式一的正极可以包括正极集流体和正极活性物质。在本发明的实施方式一的正极中,对所述正极集流体没有特殊限制,本领域技术人员可根据需要适当选择。正极集流体通常作为电子传导和收集的载体,不参与电化学反应,即在电池工作电压范围内,正极集流体能够稳定的存在于电解液中而基本不发生副反应,从而保证电池具有稳定的循环性能。正极集流体的大小可根据电池的使用用途来确定。例如,如果在要求高能量密度的大型电池中使用,则可以使用面积大的正极集流体。对正极集流体的厚度没有特殊限制,通常为1~100μm左右。对于正极集流体的形状没有特别地限定,例如可以为长方形或圆形。对构成正极集流体的材料没有特殊限制,例如,可以采用金属、合金、碳基材料等。具体地,碳基材料可以是选自玻璃碳、石墨、碳毡、碳纤维、或具有3d双连续结构的导电材料中的一种。其中,具有3d双连续结构的导电材料包括但不仅限于泡沫碳。石墨包括但不仅限于石墨箔和石墨板。金属可以是选自al、fe、cu、pb、ti、cr、mo、co、ag或经过钝化处理的上述金属中的一种。合金可以是选自不锈钢、铝合金、ni合金、ti合金、cu合金、co合金、ti-pt合金、pt-rh合金或经过钝化处理的上述合金中的一种。不锈钢包括不锈钢箔或不锈钢网,具体地,不锈钢的型号可以是但不限于300系列的不锈钢,如不锈钢304、316、316l或316p。铝合金的型号可以是但不限于6000系列的铝合金,如铝合金6061。在本发明的实施方式一的正极中,所述正极集流体上形成有正极活性物质层。所述正极活性物质层可以形成于所述正极集流体的一面,也可以形成于所述正极集流体的两面。在本发明的实施方式一正极中,对所述正极活性物质没有特殊限定,只要其能可逆脱出-嵌入金属离子即可,本领域技术人员可根据需要适当选择。在所述金属离子为锂离子的情况下,作为所述正极活性物质可以包含选自以通式li1+xmnymzok(其中,-1≤x≤0.5,1≤y≤2.5,0≤z≤0.5,3≤k≤6,m为选自na、li、co、mg、ti、cr、v、zn、zr、si、al中的至少一种)表示的具有尖晶石结构的化合物、以通式li1+xmym′zm″co2+n(其中,-1<x≤0.5,0≤y≤1,0≤z≤1,0≤c≤1,-0.2≤n≤0.2,m,m′,m″分别选自ni、mn、co、mg、ti、cr、v、zn、zr、si或al中的至少一种)表示的具有层状结构的化合物、以及以通式lixm1-ym′y(xo4)n(其中,0<x≤2,0≤y≤0.6,1≤n≤1.5,m选自fe、mn、v或co,m′选自mg、ti、cr、v或al的中至少一种,x选自s、p或si中的至少一种)表示的具有橄榄石结构的化合物中的一种或两种以上。优选地,所述正极活性物质可以包含选自limn2o4、lifepo4和licoo2中一种或两种以上。在所述金属离子为钠离子的情况下,作为所述正极活性物质,可以列举出例如:作为层状氧化物类材料的钠铁复合氧化物(nafeo2)、钠钴复合氧化物(nacoo2)、钠铬复合氧化物(nacro2)、钠锰复合氧化物(namno2)、钠镍复合氧化物(nanio2)、钠镍钛复合氧化物(nani1/2ti1/2o2)、钠镍锰复合氧化物(nani1/2mn1/2o2)、钠铁锰复合氧化物(na2/3fe1/3mn2/3o2)、钠镍钴锰复合氧化物(nani1/3co1/3mn1/3o2)、它们的固溶体、非化学计量组成的化合物等。此外,还可以列举出钠锰复合氧化物(namn2o4)、钠镍锰复合氧化物(nani1/2mn3/2o2)等。此外,还可以列举出例如作为橄榄石类材料的钠铁磷酸化合物(nafepo4)、钠锰磷酸化合物(namnpo4)、钠钴磷酸化合物(nacopo4)等。此外,还可以列举出例如作为氟化橄榄石类材料的na2fepo4f、na2mnpo4f、na2copo4f等。在目前电池工业中,几乎所有正极活性物质都会经过掺杂、包覆等改性处理。但掺杂,包覆改性等手段造成材料的化学通式表达复杂,如limn2o4已经不能够代表目前广泛使用的“锰酸锂”的通式,而应该以通式li1+xmnymzok为准,广泛地包括经过各种改性的limn2o4正极活性物质。同样的,lifepo4以及licoo2也应该广泛地理解为包括经过各种掺杂、包覆等改性的,通式分别符合lixm1-ym′y(xo4)n和li1+xmym′zm″co2+n的正极活性物质。实施方式一的正极活性物质为能可逆脱出-嵌入锂离子的物质时,优选可以选用如limn2o4、lifepo4、licoo2、limxpo4、limxsioy(其中m为一种变价金属)等化合物。此外,正极活性物质为能可逆脱出-嵌入钠离子的物质时,优选可以选用navpo4f等。正极,还包括负载正极活性物质的正极集流体,正极集流体的材料选自碳基材料、金属或合金中的一种。在具体的实施方式中,制备实施方式一的正极时,除了正极活性物质之外,根据实际情况,可能还需添加正极导电剂和正极粘结剂来提升正极的性能。正极导电剂选自导电聚合物、活性碳、石墨烯、碳黑、石墨、碳纤维、金属纤维、金属粉末、以及金属薄片中的一种或多种。正极粘结剂可以选自聚乙烯氧化物、聚丙烯氧化物、聚丙烯腈、聚酰亚胺、聚酯、聚醚、氟化聚合物、聚二乙烯基聚乙二醇、聚乙二醇二丙烯酸酯、聚乙二醇二甲基丙烯酸中的一种、或上述聚合物的混合物及衍生物。更优选地,正极粘结剂选自聚四氟乙烯(ptfe)、聚偏氟乙烯(pvdf)或丁苯橡胶(sbr)。在本发明实施方式二中,正极为碳电极或复合氧化物电极碳电极,也可以为石墨电极。另外,正极也可以由基体和在其上附着的含有正极活性物质的膏体组成。此时的正极活性物质例如可以是溴化锌,基体为碳毡、石墨毡、碳纸或碳布的多孔导电碳材料。电池的负极发生电化学反应的物质为负极反应金属,负极反应金属能够氧化溶解为负极金属离子且负极金属离子能可逆还原沉积为负极反应金属。在实施方式一或二中,负极包括负极集流体,并且负极集流体仅作为电子传导和收集的载体,不参与电化学反应。此时,负极集流体为用于负极充放电的载体。负极集流体的材料选自金属ni、cu、ag、pb、mn、sn、fe、al或经过钝化处理的上述金属中的至少一种,或者单质硅,或者碳基材料,其中,碳基材料包括石墨材料,比如商业化的石墨压制的箔,其中石墨所占的重量比例范围为90~100%。负极集流体的材料还可以选自不锈钢或经钝化处理的不锈钢。不锈钢包括但不仅限于不锈钢网和不锈钢箔,同样的,不锈钢的型号可以是300系列的不锈钢,如不锈钢304或者不锈钢316或者不锈钢316l。在一个优选实施方式中,负极除了负极集流体,还包括负载在负极集流体上的负极活性物质。此时,负极活性物质为用于负极充放电的载体。负极活性物质为锌。在一个优选实施方式中,直接采用锌片作为负极,锌片既作为负极集流体,同时也为负极活性物质。此时,锌片为用于负极充放电的载体。在本发明中,电池可以不含隔膜。当然,为了提供更好的安全性能,优选在电解液中位于正极与负极之间还设有隔膜。隔膜可以避免其他意外因素造成的正负极相连而造成的短路。本发明的隔膜没有特殊要求,只要是允许电解液通过且电子绝缘的隔膜即可。有机系锂离子电池采用的各种隔膜,均可以适用于本发明。隔膜还可以是微孔陶瓷隔板等其他材料。本发明中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。下面结合实施例,更具体地说明本发明的内容。应当理解,本发明的实施并不局限于下面的实施例,对本发明所做的任何形式上的变通和/或改变都将落入本发明保护范围。在本发明中,若非特指,所有的百分比均为重量单位,所有的设备和原料等均可从市场购得或是本行业常用的。实施例以下,通过实施例对本发明进行更具体的说明,但本发明不受这些实施例的限制。实施例1电解液1-1的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m,进一步向去离子水中添加mgso4,并使其浓度为0.01m。电解液1-2的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m,进一步向去离子水中添加mgso4,并使其浓度为0.05m。电解液1-3的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m,进一步向去离子水中添加mgso4,并使其浓度为0.25m。电解液1-4的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m,进一步向去离子水中添加mgso4,并使其浓度为0.5m。对比电解液1的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m。swagelok电池的制备将正极活性物质锰酸锂lmo、粘结剂羟甲基纤维素cmc、丁苯橡胶sbr、以及导电剂石墨ks15按照质量比84.5:1.5:2:12在水中混合,形成均匀的正极浆料。将正极浆料涂覆在正极集流体上形成活性物质层,随后将其进行压片,制成正极片,活性物质lmo的面密度为250g/m2,面积为1cm2。电解液采用上述电解液1-1、1-2、1-4,负极采用锌箔,隔膜采用玻璃纤维隔膜agm,制备swagelok电池。对应的swagelok电池,分别记为b1、b2、b4。采用相同正极、负极、隔膜以及对比电解液1制备swagelok电池,记为s1。性能测试:针对swagelok电池b1、b2、b4以及对比例s1,首先在室温下充放电循环3次后标定容量,然后将电池静置24小时,分别测量了室温下的开路电压(ocv)和容量保持率,结果如表1所示。表1swagelok蓄电池室温下的开路电压(ocv)和容量保持率。电解液ocv(v)容量保持率s11.9693%b1(0.01m)1.9793%b2(0.05m)1.9895%b4(0.5m)2.0197%如表1中所示,开路电压(ocv)随着添加剂离子mg离子浓度的增加而增加。加入0.5m镁离子的b4电池的开路电压在2.01v,比s1电池的开路电压高出约50mv,而放电容量损失仅为3%,低于s1的放电容量损失7%,放电容量损失的降低的幅度达到了57%。加入0.05m的mg离子的b2电池的ocv提高到1.98v,与s1电池相比,开路电压提高了约20mv。同时,b2的放电容量损失为约5%,而s1的放电容量损失为7%,b2的放电容量损失减小到s1的70%左右。可以理解的是,电池的容量保持率提升了,表明电池的自放电率和正极导电剂碳的损失均有减少。从电池的反应原理看,锂离子的尺寸相对小,能够在充放电的过程中自由的在锰酸锂的晶体结构中移动。而如na离子、mg离子、al离子等添加剂离子的尺寸相对而言较大,不能够嵌入锰酸锂的晶体结构中,因此,电池的比容量不会因为增加了这些添加剂离子而增大,但是,这些添加剂离子能够在电解液中自由移动,会阻碍锂离子的移动通道。因此,锂离子的脱出-嵌入的电池自放电反应速度降低了。另一方面,添加剂离子提升了氧的析出电位,减缓了电池中的其他离子可能与氧反应产生氧化物的副反应的发生。循环性能测试将电池b1、b3、b4在常温下,以3c倍率在1.4v~2.1v电压范围内进行充放电循环测试,测试结果如图1~3所示。充放电倍率高时,具有mg离子添加剂的电池表现出较好的循环性能。如图1-3所示,高的放电倍率下,需要花费大约50个循环实现稳定放电容量。放电容量稳定后,能够在几百周的循环中保持放电容量的波动不超过5%。而s1中,300个循环周期后的容量保持率仅为80%。因此,添加mg离子,电池的循环寿命和稳定性获得了显著的提升。预期电池在1000个循环之后仍然能够有95%的循环保持率。对测试电池进行内部拆解,可以看到,800个循环周期内,带有mg离子添加剂的电池未发现枝晶的现象,而没有mg离子添加剂的电池在100~300个循环周期左右,发现枝晶现象。进一步,针对电池b1和s1分别以0.2c和1c的倍率进行充放电循环测试,电压范围为1.4v~2.1v。1c倍率下电池b1和s1在50、100以及150个循环后的容量保持率,结果显示在表2中。与s1相比,b1电池的1c倍率下的比容量略有下降,但在100个循环和150个循环后,b1的容量保持率明显优于s1的容量保持率,可见添加了mg离子后,显著地提高了电池的循环性能。表2实施例2电解液2的制备称取一定量的li2so4和znso4溶于去离子水中,并使li2so4和znso4的浓度分别为1m和2m,进一步向去离子水中添加一定量的mnso4,并使mnso4的浓度为0.8m。电池的制备采用与电池b1相同的正极、负极、隔膜,并以电解液2为电解液制备电池swagelok电池,记为b5。性能测试:将电池b5在常温下,以0.2c倍率充放电,其中充电截止电压为2.1v,放电截止电压为1.4、1.2、1.0、0.5直到0v。测定得到的电池的充放电曲线。针对实施例2的电池,从图4的放电曲线中可以看出,如果放电到1.4v,放电曲线有两个充放电平台,电池的比容量为110mah/g。如果放电到0.5v左右,在小于1.4v时出现了一个新的放电平台,电池的比容量约为180mah/g,可见添加了mn离子后,电池可以实现深度放电。电池b5在常温下以0.2c倍率充放电,测量电池循环性能。放电到0.5v的结果如图5所示。以0.2c倍率放电至0.5v,电池的容量保持在160-180mah/g之间超过20个循环周期。将电池s1和b5在常温下以3c倍率充放电,测量电池充放电循环性能,结果分别如图6和7所示。根据图6和7可以知道,在50个循环之后,b5和s1的容量彼此接近。可见mn离子加入电解液中时,所增加的额外容量会保持约50个循环。高的放电倍率下,加入mn离子的电池的库伦效率更好,表明在高的放电倍率下的电池副反应减少了,正极活性材料lmo主要被还原为可逆产物。伴随着电解液中mn离子的添加,固态lmo的反应速度没有电解液中的mn离子的反应速度块,因此,在高倍率情况下,电解液中的mn离子优先参与了反应。还需要说明的是,在可实施且不明显违背本发明的主旨的前提下,在本说明书中作为某一技术方案的构成部分所描述的任一技术特征或技术特征的组合同样也可以适用于其它技术方案;并且,在可实施且不明显违背本发明的主旨的前提下,作为不同技术方案的构成部分所描述的技术特征之间也可以以任意方式进行组合,来构成其它技术方案。本发明也包含在上述情况下通过组合而得到的技术方案,并且这些技术方案相当于记载在本说明书中。以上通过具体实施方式和实施例对本发明进行了说明,但本领域技术人员应该理解的是,这些并非意图对本发明的范围进行限定,本发明的范围应由权利要求书确定。工业实用性根据本发明的电解液及电池,可以实现良好的容量保持率,放电电容损失低,并且能够实现深度放电。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1